Cette question m’est venue suite à un tweet de Frédéric Mouquet, mon ami insuffisant cardiologue lillois, qui m’a interpelé un samedi matin (quelle idée !) sur une étude sur laquelle je vais revenir. De fil en aiguille, un référence en appelant une autre, cette question de la dose optimale d’IEC pour la prise en charge de l’insuffisance cardiaque (IC) à FEVG altérée est à l’origine des deux articles précédents (sur l’histoire des IEC et sur le choix des molécules)…
La question qui se pose maintenant est la suivante : il y a-t-il un gain quelconque à chercher à tout prix à atteindre la dose d’IEC utilisée dans les études ? Est-ce une vraie perte de chance pour le patient si j’interromps l’augmentation des doses à mi-chemin ? Le patient est-il mieux traité avec 20 mg d’ENALAPRIL qu’avec 10 mg ?
Les effets secondaires des IEC surviennent précocement après l’initiation du traitement, alors que les effets bénéfiques mettent plusieurs semaines voire plusieurs mois à se matérialiser. Sans compter que l’effet hypotenseur des IEC ne serait pas très bien toléré chez des patients IC ayant souvent une pression artérielle basse si le traitement était initié d’emblée à pleine dose. Toutes les études analysant un IEC dans l’IC suivent donc le même protocole, afin de limiter les effets secondaires et d’améliorer la tolérance du traitement : initiation à faible dose et titration progressive pour atteindre la dose maximale recommandée. C’est ce même protocole que nous appliquons tous les jours quand nous prenons en charge un patient insuffisant cardiaque. Parfois, le patient ne tolère pas la dose prescrite, et il faut, au moins pour un temps, revenir à une dose inférieure. La dose au-delà de laquelle les effets secondaires sont trop handicapants est la dose maximale tolérée.
Que nous disent les grandes études randomisées ?
J’ai repris dans le tableau ci dessous les posologies utilisées dans les études ayant fondé l’utilisation des IEC dans l’IC. Premier point d’importance, dans aucune de ces études fondatrices il n’existe de comparaison de l’effet du traitement en fonction de la dose atteinte, pas même un forest plot exploratoire…
| Molécule | Dose de départ | Dose cible |
| ENALAPRIL | 5 mg x2/j (voire 2,5 mg x2/j) | 10 mg x2/j (20 mg x2/j dans CONSENSUS) |
| CAPTOPRIL | 12,5 mg x1/j | 25 mg x3/j |
| RAMIPRIL | 2,5 mg x2/j (voire 1,25 mg x2/j) | 5 mg x2/j |
| TRANDOLAPRIL | 1 mg 1x/j | 4 mg 1x/j |
Les lecteurs attentifs du billet précédent auront noté deux choses…
- que le tableau issu des recommandations de l’ESC mentionne une posologie de RAMIPRIL de 2,5 à 10 mg en une prise par jour, alors que AIRE utilisait deux prises par jour. La raison de cette discordance n’est pas expliquée dans le texte. Deux prises par jour, en plus de correspondre au protocole de l’étude, est une posologie probablement mieux tolérée qu’une seule prise par jour.
- que ce tableau contient également une ligne pour le LISINOPRIL, dont je n’ai pas encore parlé. Il est donc temps de combler ce vide.
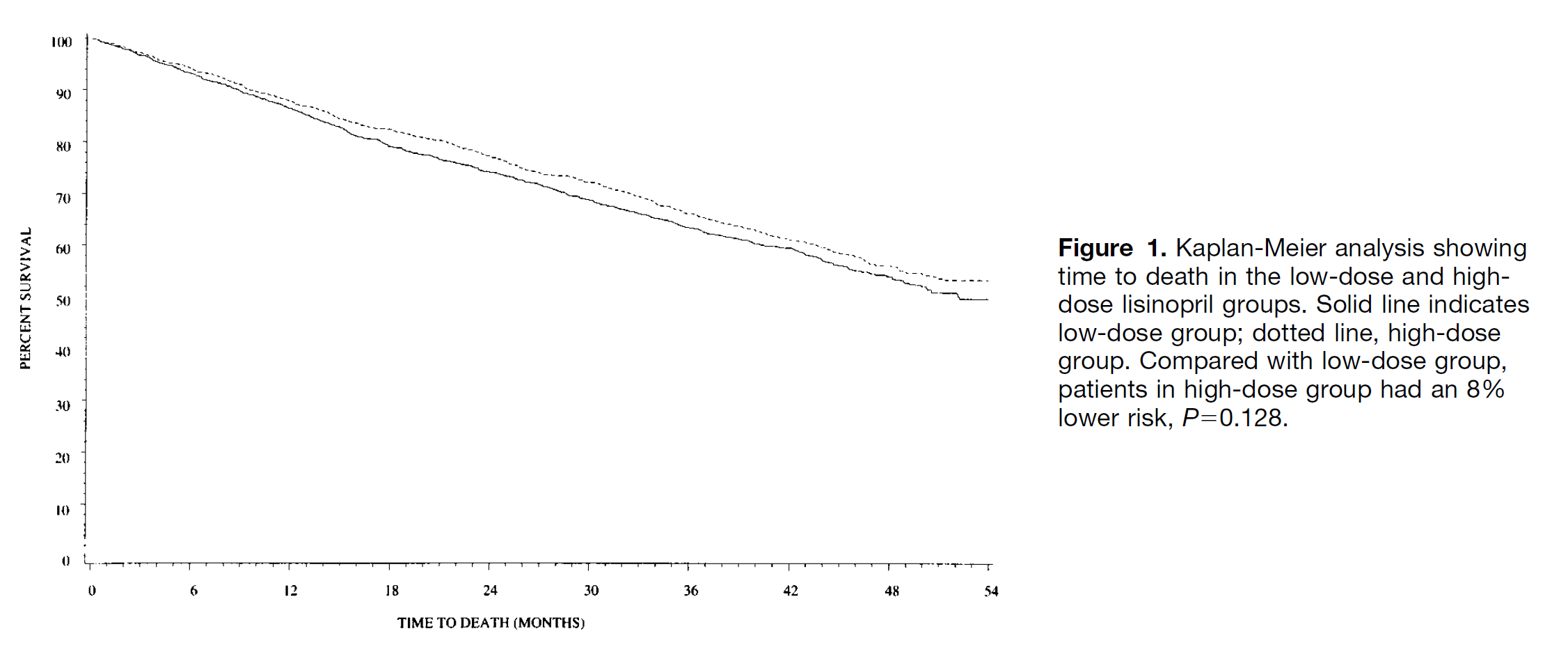
Il n’y pas, à proprement parler, d’étude de mortalité avec le LISINOPRIL dans l’IC à FEVG altérée (et c’est pour cela que je ne l’utilise pas dans cette indication – c’est par contre l’IEC utilisé dans l’étude COURAGE dont je parle ici). En effet, aucun essai clinique ne compare le LISINOPRIL au placebo dans l’IC à FEVG altérée. L’étude ATLAS compare, de manière randomisée et en double aveugle, chez plus de 3.700 patients, une faible dose (5 mg par jour) à une forte dose de LISINOPRIL (35 mg par jour) ; mais il n’y pas de groupe placebo. Après un suivi médian de 45 mois, le critère primaire, la mortalité totale, est similaire dans les deux groupes (44,9 % dans le groupe faible dose contre 42,5 % dans le groupe forte dose ; RRR 8 % ; p 0,12). Quand bien même le « critère secondaire prioritaire » de décès toutes causes et hospitalisation pour IC (que le comité scientifique a ajouté en cours de protocole et a un temps hésité à mettre en critère primaire) est significativement abaissé dans le groupe traité à haute dose (60,4 % contre 55,1 % ; RRR 12 % ; p = 0,002), cela reste purement hypothétique en l’absence de positivité du critère primaire…
Pour quelles raisons cet essai est-il neutre et échoue à justifier un traitement par forte dose ? Il y a pourtant plus d’évènements et la mortalité est plus importante dans ATLAS que dans SOLVD (sur laquelle les auteurs s’étaient basés pour calculer la puissance de l’étude) : 666 patients soit 42 % de décès dans le groupe forte dose de l’étude ATLAS après 45 mois de suivi, contre 452 patients soit 35 % dans le groupe ENALAPRIL de SOLVD après 41 mois de suivi médian. L’échec d’ATLAS tient peut-être au fait que 89% des patients étaient sous IEC avant de commencer le protocole (le détail plus précis des traitements n’est malheureusement pas disponible), alors que les patients de SOLVD devait être naïfs de traitement par IEC. Ou peut-être que le LISINOPRIL est moins efficace que l’ENALAPRIL pour la prise en charge de l’IC voire tout simplement inefficace dans l’IC ; mais ceci est impossible à affirmer en l’absence de groupe placebo.
Les méta-analyses
Il n’y a pas eu d’autre étude de grande ampleur qu’ATLAS sur ce sujet, bien que de multiples petites études ont été réalisées pour tenter de résoudre la question de la dose d’IEC. En 2017 puis tout récemment, en février 2019, paraissent deux méta-analyses (ici en 2017 et là en 2019) de ces essais pour comparer l’effet de faibles et de fortes doses d’IEC.
Les études princeps (CONSENSUS, SOLVD, SAVE, AIRE, TRACE) ne sont pas incluses dans ces méta-analyses qui ne comprennent que les études comparant différentes doses de traitement. Dans les deux cas, les conclusions sont proches : sur plus de 5.000 patients, un traitement à forte dose ne permettrai pas de diminuer la mortalité totale par rapport à un traitement à faible dose. Il y a peut-être un effet sur la mortalité cardiovasculaire ; les fortes doses par IEC permettent en revanche de diminuer le risque d’aggravation de l’IC…
Ces deux méta-analyses ont cependant les mêmes problèmes fondamentaux :
- Les études sont hétérogènes sur un point important : le prétraitement par IEC. En effet dans certaines études, les patients étaient naïfs de traitements (par exemple HEDS) ou bien il y avait une période de wash out (par exemple NETWORK), pour d’autres les patients étaient répartis entre les différentes doses alors qu’ils étaient jusque-là traités par IEC (c’est le cas notamment de 89 % des patients d’ATLAS et de 100 % des patients de l’étude de Pacher ; et pour certaines études, nous n’avons tout simplement pas l’information. Il y a dans ces méta-analyses 50 % des patients sous traitement au long cours par IEC au moment de la randomisation. Or il faut rappeler que dans SAVE notamment, les auteurs ont bien montré que les patients déjà traité par IEC avant d’entrer dans le protocole, avait un bien meilleur pronostic avec notamment une diminution de la mortalité plus importante…
- A l’exception d’ATLAS, le suivi est bien plus court dans ces études de dose que dans les études de mortalité telles que SOLVD-treatment ou SAVE (suivi médian de 40 mois dans les deux cas). Le suivi pour l’étude de Pacher ou pour HEDS était de 48 semaines, dans NETWORK de 24 semaines. Si le bénéfice des IEC en terme de mortalité s’installe en quelques semaines en comparaison du placebo, le bénéfice d’une forte dose d’IEC par rapport à une dose plus faible est peut être plus long à s’installer ?
- ATLAS pèse 90 % des événements et 54 % des patients de ces méta-analyses. Autant dire qu’il est difficile de faire dire autre chose que le résultat d’ATLAS. Ce qui renforce encore le poids du groupe de patients sous traitement par IEC au moment de la randomisation…
- les études ayant démontré une efficacité sur la mortalité totale ne sont pas incluses dans l’analyse…
Que conclure ?
En l’état actuel des données, il semble difficile de justifier de fortes doses d’IEC si un patient ressent des effets secondaires handicapants ; surtout pour un traitement pris à vie dans l’immense majorité des cas. J’insiste sur ce fait : en cas de symptômes handicapants.
Les études fondatrices ont obtenu les résultats positifs que l’on connait en titrant le traitement pour atteindre la dose la plus haute possible, et il faut suivre cette stratégie en raison de l’importance du gain en termes de survie qu’apporte ces traitements.
Il est néanmoins possible qu’une part substantielle de l’effet bénéfique des IEC soit obtenue dès le premier palier, et que la titration « automatique » ultérieure n’apporte qu’une amélioration modeste du pronostic, ou sur des critères moins « durs » que la mortalité totale, par exemple les hospitalisations pour insuffisance cardiaque ou la classe fonctionnelle. C’est la conclusion notamment de deux analyses post-hoc de SOLVD-treatment parues en 2017 et en 2020. Il n’est pas exclu également que seuls certains sous-groupes de patients bénéficient d’une forte dose de traitement.
Les points importants sont donc pour moi
- Il vaut mieux une faible dose que pas d’IEC du tout
- Il n’y a probablement pas de bénéfice à une dose d’IEC supérieure à celle testée dans une des études de mortalité
- S’il faut chercher à atteindre la dose maximale, il faut savoir redescendre d’un pallier si les effets indésirables sont trop gênants. La perte de chance en termes de mortalité est probablement minime et le/la patient.e y gagnera en qualité de vie.
- Il vaut peut-être mieux une dose plus faible d’IEC mais permettant d’introduire de la SPIRONOLACTONE qu’une pleine dose d’IEC sans SPIRONOLACTONE (simple supposition de ma part, il n’y a pas d’essai validant ou non cette hypothèse – à ma connaissance).
- Si le bénéfice des IEC est majeur dès les premières doses, il vaut mieux faire une titration en parallèle des bêtabloquants et des IEC que de monter l’un au maximum avant d’introduire le deuxième.


Alors pour le ramipril dans l’IC tu préconises en une ou deux prises par jour (surtout pour une population gériatrique très fragile et très polypathologique?)
J’aimeJ’aime
Clairement deux prises par jour, ça permet de donner en une fois une dose moins importante et donc d’éviter un peu plus les hypotensions.
Les patients supportent mieux (expérience perso, je n’ai pas regardé s’il y avait des données la dessus) 10 mg en deux prises que 10 mg en une prise, même donnée le soir
J’aimeJ’aime
une fois encore merci pour ces explications très claires !
J’aimeJ’aime