Contexte
L’une des présentations les plus attendues du millésime 2019 du congrès de l’ESC (European Society of Cardiology), en tout cas dans le domaine de l’insuffisance cardiaque, était celle de l’étude PARAGON. PARAGON (Prospective Comparison of ARNI with ARB Global Outcomes in HF With Preserved Ejection Fraction) est un essai de phase III sponsorisé par NOVARTIS visant à évaluer l’efficacité de l’association SACUBITRIL/VALSARTAN dans l’insuffisance cardiaque à FEVG préservée (ICFEP). Cette association thérapeutique, disponible en France sous le nom d’ENTRESTO® a fait ses preuves dans l’IC à FEVG altérée (ICFEA) dans le cadre de l’étude PARADIGM (je ne reviendrai pas ici sur les critiques positives et négatives que l’on peut faire de cet essai). L’ICFEP est un syndrome fréquent (environ 50 % des insuffisances cardiaques) pour lequel il n’existe pas de thérapeutique ayant démontré une efficacité en termes de réduction de la mortalité. Beaucoup d’espoirs étaient placés dans cette étude. Une étude de phase 2, l’étude PARAMOUNT, s’était révélée positive dans cette pathologie, avec la même molécule et un critère primaire intermédiaire : l’évolution du taux de NT-proBNP à 12 semaines. Pour faire court, PARAMOUNT comparait deux groupes de 149 et 152 patients traités respectivement par SACUBITRIL/VALSARTAN ou VALSARTAN. Le NT-proBNP passait de 783 pg/mL [95% CI 670–914] à 605 pg/mL [512–714] dans le groupe SACUBITRIL/VALSARTAN, et de 862 pg/mL [733–1012] à 835 [710–981] pg/ml dans le groupe VALSARTAN (p=0,005).
Mais le 29 juillet dernier, NOVARTIS a publié un communiqué de presse annonçant que cette étude « échouait de peu à démontrer une supériorité statistique sur le critère primaire ». Les commentaires et discussions ont été nombreux suite à cette annonce, et la présentation des résultats était attendue avec impatience.
PARAGON a donc été présentée le 1er septembre lors du congrès de l’ESC, et publiée concomitamment dans le NEJM.
Design de l’étude
Le design de l’étude avait déjà été publié ici, et les caractéristiques des patients à l’inclusion ici
Les patients inclus étaient des patients de plus de 50 ans, avec une FEVG supérieure ou égale à 45 %, symptomatiques (NYHA 2 à 4), nécessitant un traitement diurétique depuis au moins 30 jours, avec un NT-proBNP supérieur à 200 pg/ml en cas d’hospitalisation pour IC dans les 9 derniers mois, ou supérieur à 300 pg/ml dans le cas contraire. Ces chiffres minimums étaient multipliés par 3 en cas de fibrillation atriale. Les patients devaient en outre avoir des signes d’atteinte structurelle cardiaque (hypertrophie ventriculaire ou dilatation atriale gauche). Parmi les critères d’exclusion, notons l’existence d’une mesure antérieure de la FEVG inférieure à 40 % (ce qui permet d’éviter d’inclure des patients ayant une ICFEA ayant récupéré), une IC décompensée au moment de l’inclusion, les patients avec cardiopathie chimio-induite, dilatée ou du péripartum, avec cardiopathie hypertrophique génétique ou infiltrative, valvulaire ou congénitale.
Les patients étaient inclus dans une période de run-in pendant laquelle ils prenaient du VALSARTAN (40 ou 80 mg 2 fois par jour) pendant 1 à 2 semaines, puis 1 à 2 semaines du SACUBITRIL/VALSARTAN (49/51 mg deux fois par jour). Les patients tolérant les deux molécules étaient alors randomisés entre VALSARTAN 160 mg deux fois par jour ou SACUBITRIL/VALSARTAN 97/103 mg deux fois par jour. Les autres traitements pouvaient être poursuivis, à l’exception des traitements par IEC ou ARA2. Rappelons que les 103 mg de VALSARTAN présents dans l’association SACUBITRIL/VALSARTAN permettent d’obtenir une concentration plasmatique équivalente à 160 mg de VALSARTAN classique. Contrairement à PARADIGM qui comparait plutôt une stratégie thérapeutique (SACUBITRIL/VALSARTAN vs ENALAPRIL), PARAGON permet d’étudier l’apport du SACUBITRIL par rapport au VALSARTAN seul (sans présager de l’intérêt de cette molécule dans l’ICFEP…).
Le critère primaire composite comprend les hospitalisations TOTALES (premier épisode et épisodes récurrents) pour insuffisances cardiaque et la mortalité cardiovasculaire, ce qui change des études précédentes qui prenaient en compte le premier événement du critère primaire. Les auteurs justifient ce choix par le fardeau que représente les hospitalisations itératives chez les patients avec IC. Les critères secondaires sont l’amélioration des symptômes et de la qualité de vie à 8 mois (score KCCQ), l’amélioration de la classe NYHA à 8 mois, le ralentissement de la dégradation de la fonction rénale et le ralentissement de la mortalité toute cause. Tous les critères étaient adjudiqués en aveugle, sauf… le score KCCQ et la classe NYHA ; ce qui, pour des critères fonctionnels subjectifs, en ôte une certaine valeur…
Résultats
Sur plus de 10.000 patients potentiels, 5.746 ont été inclus dans la phase de run-in. 4.822 seront finalement randomisés, les patients exclus l’étant majoritairement pour non-tolérance (hypotension, hyperkaliémie, insuffisance rénale) du VALSARTAN (340 patients) ou du SACUBITRIL/VALSARTAN (262 patients) ; soit 10 % d’intolérance à l’un des deux composés. Les patients exclus sont un peu différents des patients finalement randomisés : ils sont plus âgés, plus dyspnéiques, ont plus de comorbidités, ont une fréquence cardiaque plus élevée et une pression artérielle plus basse, ont été plus souvent hospitalisés pour insuffisance cardiaque et ont un NT-proBNP plus élevé – cette dernière différence me semble particulièrement intéressante (1.062 [998 – 1.129] pg/ml vs 885 [863 ; 908] pg/ml ; p < 0,001). Au plan thérapeutique, les patients exclus sont moins souvent traités par IEC/AR2 ou bétabloquant, mais plus souvent sous antagoniste des récepteurs minéralocorticoïdes (ARM) (spironolactone, eplerenone). La proportion de traitement diurétique est la même.
Que dire de la population finalement incluse dans l’étude ? Elle est plutôt âgée (72 ans), sans majorité féminine (51 % – alors que l’ICFEP est traditionnellement considérée comme ayant une population féminine prédominante), obèse (IMC 30 kg/m²). La cause de l’IC est dans un peu plus d’un tiers des cas une cardiopathie ischémique. La FEVG est de 57 %. Le NT-proBNP médian est de 900 pg/ml, (avec cependant une borne inférieure de l’intervalle interquartile à 470 pg/ml) et les patients sont très majoritairement en classe II de la NYHA. 39 % avait déjà été hospitalisés pour IC. 95 % des patients présentent une hypertension artérielle. 95 % des patients est traité par diurétique, 85 % étaient sous IEC ou ARA2 avant l’étude, 80 % sous bétabloquant et 25 % sous ARM. La durée médiane de suivi est de 35 mois.
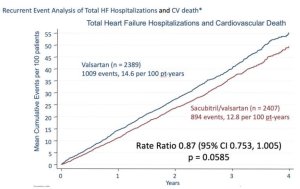
Le groupe VALSARTAN (2.389 patients) présente 1.009 événement (797 hospitalisations et 212 décès, chez 526 patients) soit 14,6 pour 100 patients-années, le groupe SACUBITRIL/VALSARTAN 894 événements (690 hospitalisations et 204 décès, chez 526 patients) soit 12,8 pour 100 patients-années, soit une réduction relative de 0,87 (95% CI 0,753 – 1,005) pour un p à 0,0585. Or l’étude a été dimensionnée pour un taux d’événements de 9 pour 100 patient-années. L’échec de l’étude ne vient donc pas de sa puissance. Si le nombre total d’hospitalisations est plus bas dans le groupe SACUBITRIL/VALSARTAN, cette différence n’est pas significative non plus (RR 0.85 (0.72–1.00)). En regardant les appendices, il est intéressant de constater que, si on prend le critère plus classique « première hospitalisation pour IC ou décès cardiovasculaire », le bénéfice est encore moins important et moins significatif (HR = 0.917 (0.814 –1.033)). Les décès toutes causes sont de 342 (14,2 %) dans le groupe SACUBITRIL/VALSARTAN et 349 (14,6 %) dans le groupe VALSARTAN.
Bien évidement de multiples analyses de sous-groupe ont été réalisées. Rappelons encore une fois qu’avec un critère primaire neutre, elles n’ont pas d’autre valeur que de donner quelques idées. On observe que le bénéfice du traitement serait plus important chez les femmes et en cas de FEVG inférieure à la médiane (donc entre 45 % – critère d’inclusion – et 57 %). Ce dernier point n’est guère étonnant puisque PARADIGM est positif dans l’ICFEA (la FEVG devait être inférieure à 40 %, puis 35 % après un amendement au protocole). Les patients traités par ARM pourraient également tirer un meilleur bénéfice du traitement (selon le forest plot mais pas en analyse multivariée) mais est-ce de par l’association ARM-SACUBITRIL/VALSARTAN en elle-même, ou parce que ces patients ont une sévérité différente (les patients sortant d’hospitalisation sont notamment plus fréquemment sous ARM (30% vs 20 %)) ? On passera rapidement sur l’amélioration du score KCCQ et de la classe NYHA, cette dernière apparaissant extrêmement modeste, avec notamment dans les deux groupes 76 % patients n’ayant aucune modification (l’IC est une maladie générale et la dyspnée multifactorielle, et il y a probablement plus à gagner avec le ré-entrainement sur ce point qu’avec les médicaments seuls). L’altération de la fonction rénale semble au contraire moins fréquente sous SACUBITRIL/VALSARTAN que sous VALSARTAN .
Au plan sécurité, on relève un excès d’angioedème dans le groupe SACUBITRIL/VALSARTAN (14 vs 4 patients). Notons que la pression artérielle est plus basse de 4 mmHg dans le groupe SACUBITRIL/VALSARTAN, avec plus d’épisodes de pression artérielle inférieure à 100 mmHg (15 % vs 1 %).
Qu’en penser ?
PARAGON est une déception. Nombre d’entre nous attendions beaucoup de cette étude et du SACUBITRIL/VALSARTAN pour prendre en charge les patients ayant une ICFEP. L’étude semble avoir été bien menée, les résultats robustes.
Peu à dire au plan statistique
On voit déjà fleurir les commentaires arguant que l’étude est « presque positive« . Le critère primaire a été choisi pour augmenter la puissance statistique par rapport aux études précédentes, et le taux d’événement a été supérieur à ce qui été prévu. L’étude est donc de taille suffisante. L’étude aurait-elle pu être positive avec un suivi prolongé ? Peut être, mais cela aurait-il eu un impact clinique ? Le suivi médian est de 3 ans, et le seul bénéfice porterait au mieux sur les nombre total d’hospitalisations, et non sur les décès ou le premier épisode d’hospitalisation. Difficile d’y voir un intérêt dans une pathologie dont la mortalité serait de 20 % à un an et 50 % à 5 ans (Dunlay et al.).
Et évidement en parallèle commencent les discussions sur les analyses de sous-groupes. Mon avis est qu’on ne devrait même pas faire ni publier ces analyses ; cela éviterait certaines tentations. Statistiquement elles sont sans fondement. Mais si on les regarde (puisqu’elles ont été faites, et que tout le monde en parle..), rien d’étonnant à ce que le SACUBITRIL/VALSARTAN semble fonctionner d’autant mieux qu’on se rapproche d’un tableau d’ICFEA… Je n’ai guère d’avis sur l’apparente meilleure efficacité chez les femmes : l’apparente différence d’efficacité dans une analyse de sous-groupe d’une étude dont le critère primaire n’est pas atteinte peut n’être que purement fortuite…
A-t-on inclus les bons patients ?
Peut-on trouver une explication à cet échec ? Émettre des hypothèses en tous les cas. Le diagnostic d’ICFEP est difficile, mais, compte tenu des critères d’inclusion, les patients de PARAGON sont les patients les plus probablement porteurs d’une ICFEP parmi les études d’intervention pharmacologique faite dans cette pathologie (voir le tableau). Néanmoins, les pathologies qui engendrent ce syndrome sont très diverses, et la physiopathologie exacte de l’ICFEP n’est pas clairement établie. Le problème de l’amylose à transthyrétine par exemple, responsable de 10 et 15 % des ICFEP, est à mon sens un des premiers à soulever : en l’absence de dépistage, combien de patients souffrent d’amylose – à des degrés divers – dans chaque groupe ? Comment répondent-t-ils au SACUBITRIL/VALSARTAN ? Un cardiopathie hypertensive et une cardiopathie ischémique ont-elles la même réponse au traitement ? Quelle influence de la FA ? Un patient avec un antécédent d’infarctus non transmural, en FA, avec un NT-proBNP à 900 pg/ml répond-il pareillement au traitement qu’un patient avec un antécédent d’infarctus non transmural, en rythme sinusal, avec un NT-proBNP à 900 pg/ml ? Je ne le pense pas, et je ne suis même pas sûr que le premier soit véritablement de l’ICFEP… Tant que nous n’aurons pas clairement compris et déterminé ce qu’est l’ICFEP, il est difficile d’imaginer la traiter correctement.
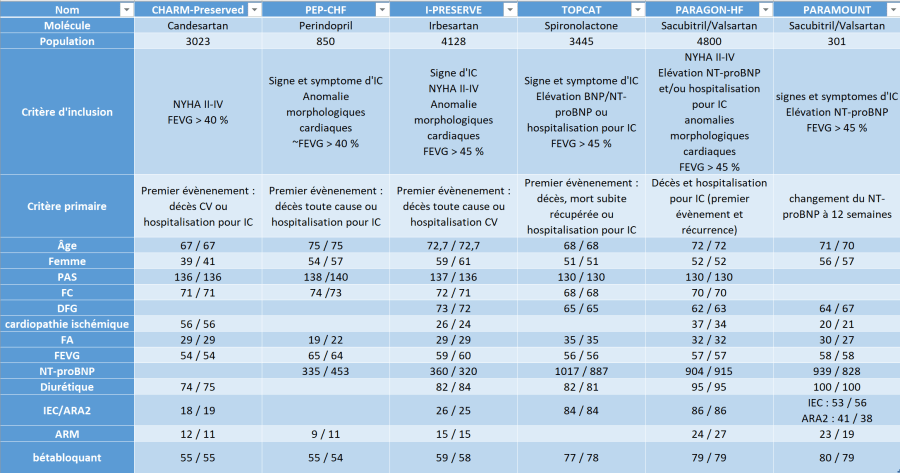
(le premier chiffre est celui du groupe contrôle, le deuxième celui du groupe traitement)
Admettons néanmoins que les patients randomisés ont bien de l’ICFEP. L’atteinte est-elle suffisamment sévère pour qu’un bénéfice thérapeutique puisse être mis en évidence ?
- Si le taux médian de NT-proBNP est l’un des plus élevés des études faites dans l’ICFEP, 25 % des patients ont un NT-proBNP inférieur à 470 pg/ml.
- Les patients ne pouvaient pas être inclus en cas de pression artérielle supérieure à 150 mmHg, sauf à avoir un traitement par 3 molécules. Quelle est la proportion de ces patients avec une HTA sévère voire résistante, qui sont normalement l’archétype de l’ICFEP ?
- 85 % des patients étaient déjà sous traitement par IEC ou ARA2, 25 % sous ARM. Le résultat aurait-il été différent avec des patients naïfs de traitement ?
- les patients exclus lors de la phase de run-in, semblant plus graves, auraient-ils une réponse différente au traitement ? En voulant s’assurer de la tolérance à des doses assez élevées de traitement, s’est-on privé de patients répondant au traitement ?
- Et puis surtout, la mortalité dans l’étude est très faible. A peine 8 % de mortalité CV, et 14 % de mortalité totale, là où on attendrait probablement 30 % selon les données épidémiologiques…
Conclusion
Ce ne sera pas la révolution SACUBITRIL/VALSARTAN dans l’ICFEP. Quelles que soient les raisons de l’échec de cette molécule, l’étude fera encore beaucoup parler. Problème de méthodologie – je ne pense pas – ou patients insuffisamment sélectionnés ou insuffisamment graves – plus probablement – il y aura matière à réflexion… De nombreuses études ancillaires et analyses post-hoc seront publiées pour tenter de trouver des explications. Souvenons-nous juste que l’étude est négative, pour ne pas s’extasier d’analyses de sous-groupes. Et d’autres études sont en cours, mais nous aurons probablement l’occasion d’y revenir
Le principal problème reste pour moi qu’on ne sait toujours pas de quoi on parle avec l’ICFEP. Derrière une apparente homogénéité syndromique, se cache une trop grande diversité de pathologie pour qu’on puisse se limiter à inclure des patients sous le label « insuffisance cardiaque à FEVG préservée », sans affiner les critères ; c’est un peu comme si on incluait dans une étude pour une chimiothérapie, des patients avec « cancer », sans spécifier « cancer du sein » ou « cancer du colon ».