STEP : contrôle intensif de la pression artérielle chez le sujet âgé.

primaire chez les personnes âgées et très âgées, Neurol psychiatr gériatr, https://doi.org/10.1016/j.npg.2021.07.004
Le leitmotiv en prévention cardiovasculaire est globalement lower is better, que ce soit pour les dyslipidémies, le diabète ou l’hypertension artérielle. La question de la cible tensionnelle à atteindre chez les patients âgés hypertendus reste un sujet de débat. Eric Maeker et moi-même discutons du sujet dans un article récent. Les variations dans les recommandations des sociétés savantes (voir le tableau ci-contre) illustrent bien qu’il n’y a pas de consensus arrêté sur la question, notamment selon la valeur que l’on donne aux résultats de SPRINT SENIOR (voir à ce sujet ce que nous en disons dans notre article, ou par exemple dans celui-ci).
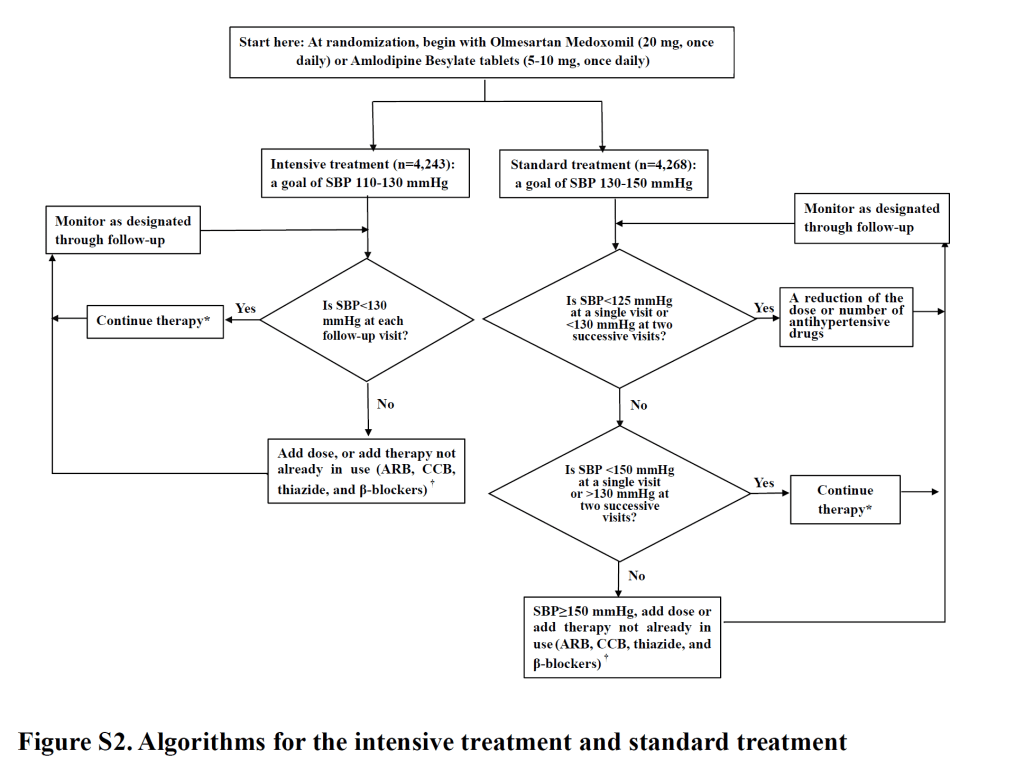
L’étude STEP (Strategy of Blood Pressure Intervention in the Elderly Hypertensive Patients) est une étude randomisée, sans aveugle, ayant inclus 8.511 patients de 60 à 80 ans pour comparer l’efficacité d’une cible tensionnelle à 110-130 mmHg par rapport à une cible à 130-150 mmHg). La PAs moyenne en fin d’étude est de 126,7 mmHg dans le groupe intensif (77% des patients à l’objectif ; 1,9 traitements) et 135,9 mmHg dans le groupe standard (76% des patients à l’objectif ; 1,5 traitements) (contre 146 mmHg initialement). Les patients pouvaient être inclus s’ils avaient une PAs entre 140 à 190 mmHg ou s’ils étaient déjà sous traitement antihypertenseur. Les patients avec antécédents d’AVC (hémorragique ou ischémique) étaient exclus. Les molécules recommandées étaient l’OLMESARTAN, l’AMLODIPINE et l’HYDROCHLOROTHIAZIDE, et le protocole d’adaptation est précisé dans les appendices (voir ci-contre).
Avec un suivi initialement prévu de 4 ans, l’étude a été interrompue prématurément après 3,3 ans pour efficacité, posant toujours le même problème méthodologique. L’étude est positive sur un critère primaire composite comprenant AVC (ischémique ou hémorragique), syndrome coronaire aigu, décompensation cardiaque, revascularisation coronaire, fibrillation atriale et décès de cause cardiovasculaire (HR 0,74 ; IC95% 0,60 – 0,92 ; p=0,007). La baisse absolue est de 1,1%, le NNT est à 91. Une fois prise en compte les différences en termes de mesure de la PA, les résultats de STEP sont assez proches de ceux de SPRINT. En effet, du fait d’une prise de PA qui s’apparentait plus à une automesure tensionnelle qu’à une mesure de consultation, les chiffres de PAs de SPRINT doivent être majorés de 10 mmHg environ ; les deux essais sont donc très proches sur ce plan là. L’analyse des composants du critère primaire de STEP montre une baisse des AVC, des syndromes coronaires et des décompensations cardiaques, sans baisse de la mortalité cardiovasculaire ou totale. La baisse de ces évènements est difficile à juger dans une étude en ouvert où le traitement par statine a peut être été différent entre les groupes, information que nous n’avons pas. SPRINT avait montré une baisse de la mortalité cardiovasculaire et totale, sans baisse des AVC ou des épisodes coronaire ; seule les décompensations cardiaques étaient diminuées, faisant dire à certains que le bénéfice dans SPRINT est possiblement lié à l’usage fréquent des diurétiques (50% de diurétique dans SPRINT contre 5% dans STEP).
STEP n’est pas un argument pour une baisse importante de la PAs chez tous les patients âgés. L’âge moyen est de 66 ans avec juste 1/4 des patients de plus de 70 ans, ne permettant pas de généraliser les résultats de cette étude à une population vraiment âgée (l’âge moyen dans SPRINT-SENIOR est de 80 ans, et de 83,5 ans dans HYVET). Les comorbidités cardiovasculaires sont peu fréquentes, surtout en comparaison de SPRINT (maladie cardiovasculaire 6% dans STEP, contre 20% dans SPRINT, dysfonction rénale 2% vs 28%). Par ailleurs, seuls des patients d’éthnie Han ont été inclus, ce qui peut poser des problèmes de transposition des résultats chez les patients occidentaux, ce que soulignent les auteurs eux-mêmes. Notons aussi que dans cette population jeune et à faible risque, les épisodes d’hypotension sont plus fréquents dans le groupe intensif (HR 1,31 ; IC95% 1,02–1,68 ; p=0,003).
A mon sens, STEP confirme ce que Eric Maeker et moi écrivions dans notre article publié dans PNG. Chez les patients de plus de 65 ans, baisser la PAs en-dessous de 130 mmHg apporte quelques bénéfices marginaux par rapport à une PAs inférieure à 140 mmHg, sans baisse de la mortalité, chez des patients très sélectionnés (notamment sans diabète ou rigidité vasculaire excessive). Il serait largement excessif – et faux – de considérer que cet étude valide une stratégie de contrôle intensif de la PA chez les patients âgés.
SSaSS : baisse des apports sodés par l’utilisation de sel de régime
La consommation de sel favorise l’élévation de la pression artérielle et majore le risque d’évènement cardiovasculaire. La diminution des apports sodés est associée à une baisse de la charge tensionnelle de manière dose-dépendante. Néanmoins, aucune étude n’a montré d’efficacité sur les évènements cliniques. L’étude SSaSS (Salt Substitute and Stroke Study) est une étude randomisée en cluster réalisée sur 600 villages en Chine visant à déterminer l’efficacité des « sels de régime » sur la baisse des accidents vasculaires cérébraux. Les sels de régime remplacent une partie du chlorure de sodium par du chlorure de potassium, ce qui peut soulever des interrogations quand au risque d’hyperkaliémie. 35 patients étaient inclus par village, et les villages randomisés entre sel de régime (25% de chlorure de potassium et 75% de chlorure de sodium) ou sel normal. 20.995 patients ayant un antécédent d’AVC ou de plus de 60 ans avec une HTA non maitrisée ont été inclus et suivis pendant 5,1 ans.
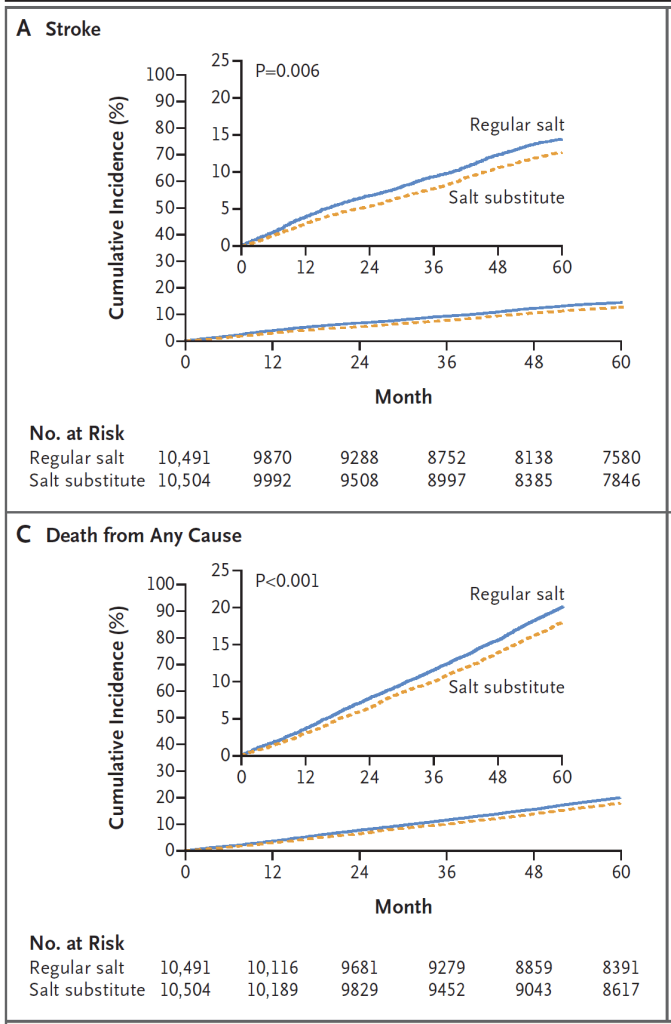
L’âge médian est de 65 ans, avec un antécédent d’AVC dans 72% des cas. La PA initiale est à 154/89 mmHg avec une consommation sodée quotidienne (estimée sur la base de la natriurèse) à 11g (ce qui est assez proche des chiffres français). On observe dans le groupe « sel de régime » une baisse de la PAs d’environ 3 mmHg et de la natriurèse de 350 mg (soit l’équivalent d’une baisse des apports en sel de 900 mg par jour). Cette amélioration tensionnelle se traduit par une efficacité clinique avec une baisse significative du risque d’AVC (critère primaire) (29,1 vs. 33.7 évènement pour 1000 personnes-années ; RR 0,86 ; IC95% 0,77-0,96 ; p=0,006). On observe également une baisse de la mortalité toute cause (critère secondaire) (RR 0,88 ; IC95% 0,82 – 0,95). L’effet est équivalent dans l’ensemble des sous-groupes.
Il n’a pas été mis en évidence de surrisque d’hyperkaliémie, mais d’une part les patients ayant une insuffisance rénale ou utilisant des traitements hyperkaliémiants (en dehors des IEC/ARA2 pris par un quart de la population de l’étude) étaient exclus de l’étude, et d’autre part il n’y a pas eu de dosage de la kaliémie au cours de l’étude. Ce dernier point ne me semble pas fondamental, car on ne traitement pas un chiffre mais un patient avec un objectif clinique. Arrêter le sel du substitution, compte tenu de l’effet clinique, pour une kaliémie un peu supérieure à 5 voire même 5,6 mM aurait-il vraiment un sens ?
Cette étude me semble vraiment importante. Elle n’est pas exempte de biais, le plus important étant qu’en l’absence d’aveugle, les patients du groupe « sel de régime » ont probablement modifié leur comportement ou leur traitement, favorisant le bénéfice sur le critère primaire. D’un autre côté, la consommation de sel de régime probablement très variable et pas systématique d’un patient à l’autre, et le fait que 6% des patients du groupe contrôle a pris du sel de régime, diminuent l’amplitude du bénéfice. Avec plus de 20.000 patients suivis plus de 5 ans et un critère primaire unique, cette étude est robuste et démontre encore une fois que la prise en charge non pharmacologique est fondamentale en médecine. Le risque d’hyperkaliémie semble très faible si ce n’est inexistant ; néanmoins je ne généraliserai pas cette absence de risque aux insuffisants cardiaques qui souvent prennent des antagonistes des récepteurs minéralocorticoïdes et présentent une altération de la fonction rénale, ni évidemment aux insuffisants rénaux (ces deux populations étant exclues de l’étude). Dernier point que je discute souvent en éducation thérapeutique, c’est que l’usage des sels de régime pose le même problème que les édulcorants avec le sucre : ils favorisent la persistance de l’appétence pour le goût salé, quand l’idéal serait de désapprendre à manger salé. Néanmoins on a là un nouvel outil de prévention cardiovasculaire, bon marché, dont l’usage à large échelle pourrait permettre de diminuer l’impact des maladies cardiovasculaires.
QUARTET : quadrithérapie à faible dose dans la prise en charge initiale de l’hypertension artérielle
L’un des principaux problème de la prise en charge de l’HTA est l’inertie thérapeutique qui ralenti l’augmentation du traitement et le contrôle de la charge tensionnelle ; les effets secondaires dont la fréquence augmente avec le dosage et le nombre de molécule sont un autre obstacle. Une des solutions pour passer outre ces deux écueils est de donner dès le début de la prise en charge un traitement par plusieurs molécules à faible dose (habituellement une bithérapie à demi-dose), permettant de limiter les effets secondaires tout en améliorant l’efficacité. Cette approche, recommandée notamment par l’ESC en 2018, n’a pas été retenue par le NICE britannique en 2019, qui juge qu’il n’y a pas de preuve évidente de la supériorité de cette stratégie par rapport à une monothérapie initiale.
L’étude QUARTET (quadruple ultra-low-dose treatment for hypertension) est une étude randomisée en double aveugle, ayant recruté des patients hypertendus naïfs de traitement (57% des patients) ou déjà sous monothérapie. 591 patients (âge moyen 59 ans, globalement à faible risque cardiovasculaire) ont été inclus sur les 650 prévus, les inclusions ont été interrompues en raison de la pandémie. L’étude comparait l’efficacité d’une quadripill (irbesartan 37,5 mg, amlodipine 1,25 mg, indapamide 0,625 mg et bisoprolol 2,5mg) face à une monothérapie par irbesartan 150 mg. En cas de PA > 140/90 mmHg à la sixième semaine, l’étape suivante était l’ajout de 5 mg d’amlodipine ; après quoi la prise en charge était laissée à la discrétion du médecin habituel du patient. A 12 semaines, 15% des patients du groupe « quadripill » avait une molécule supplémentaire, contre 40% dans le groupe contrôle (ce n’est pas systématiquement de l’amlodipine, ce qui semble être une déviation du protocole).
A 12 semaines, la quadripill permet une baisse de la PA plus importante que la monothérapie : 120/71 mmHg dans le groupe « quadripill » contre 127/79 mmHg dans le groupe contrôle (-6,9 mmHg ; IC95% -4,9 – -8,9 ; p<0,001). Un suivi à un an était proposé à tous les patients, et l’effet tensionnel est le même à ce terme. A 12 semaines, dans le groupe « quadripill » il y a significativement plus d’hypotension artérielle (PA < 100 mmHg ; 6% vs 2,5%) et de bradycardie (FC < 50 bpm ; 12,4 % vs 0,4 %), sans que l’excès d’épisodes vertigineux ne puisse être retenu comme pertinent (p=0,07) – en rappelant que l’étude est sous-dimensionnée par rapport aux prévisions d’inclusion.
Cette étude n’apporte pas grand chose à la question de la prise en charge de l’HTA. Quel intérêt de faire une quadrithérapie sans spironolactone mais incluant un bétabloquant, connaissant les résultats des études LIFE et PATHWAY-2 ? Quel intérêt de mettre un ARA2 plutôt qu’un IEC dans la quadripill alors que les données sont plus robustes avec les IEC ? Pourquoi utiliser un ARA2 comme traitement contrôle alors que les IEC sont à préférer et que Cochrane recommande un thiazidique ou éventuellement un IEC ou un inhibiteur calcique en première ligne. Quel est l’intérêt clinique d’une PAs à 120 mmHg plutôt que 127 mmHg chez des patients jeunes à faible risque cardiovasculaire ? On est largement en dessous des cibles thérapeutiques, et cette étude n’apporte aucun élément en terme de bénéfice sur les évènements cliniques. Le chiffre de PA n’est qu’un critère de substitution pris en défaut à plusieurs reprises : lower n’est pas forcément better et toutes les classes pharmacologiques n’apportent pas le même bénéfice à baisse de PA égale (illustré dans LIFE ou ALLHAT par exemple). Quelle tolérance à long terme compte tenu du surcroit d’hypotension et bradycardie dans les 12 premières semaines, et sur un nombre plus grand de patients ? Bref, comme dans l’insuffisance cardiaque, lutter contre l’inertie thérapeutique, ce n’est pas multiplier les classes pharmacologiques à petite dose en première ligne.