Dans le premier billet de ce diptyque, nous avons posé les bases conceptuelles et épidémiologiques de l’aggravation de l’insuffisance cardiaque. C’est une entité fréquente, au pronostic lourd, mais dont la prise en charge ambulatoire est déjà une réalité pour une part significative des patients. Après cette première partie théorique, le présent billet se veut plus orienté vers la pratique clinique : comment décider du lieu de soin ? quel traitement diurétique prescrire ? comment organiser le suivi pour que la prise en charge ambulatoire soit non seulement possible, mais sûre ?
Dans ce billet pratique, j’utiliserai indifféremment « aggravation de l’IC » et « décompensation cardiaque ». Les nuances sémantiques ont été discutées dans le premier billet, c’est ici la réalité clinique qui prime.
Stratification du Risque : quel patient pour une prise en charge ambulatoire ?
L’évaluation initiale du patient en décompensation ne doit pas se limiter à une simple quantification de la congestion. Il s’agit de stratifier le risque à court terme, afin de déterminer le lieu de soin et la stratégie thérapeutique les plus adaptés. Si majoritairement la réflexion va opposer prise en charge ambulatoire par voie orale et prise en charge hospitalière par voie intraveineuse, il ne faut pas oublier que se développent dans de nombreux endroits, des structures permettant de faire un traitement diurétique intraveineux en hôpital de jour, voire en hospitalisation à domicile, qui sont autant d’alternatives à l’hospitalisation conventionnelle.
La prise en charge hospitalière se comprend tout à fait dans une volonté de prudence et/ou de praticité. L’hôpital offre un cadre contrôlé qui facilite la prise en charge : surveillance rigoureuse de la diurèse et de l’évolution pondérale, contrôle strict des apports sodés, meilleure adaptation des doses des diurétiques notamment sur la base de la natriurèse. En outre, la littérature étayant la prise en charge en ville est très limitée. Les études se concentrent en général sur les patients stabilisés pour l’évaluation de l’optimisation du traitement de fond, ou sur les patients décompensés mais hospitalisés. Les deux seuls essais randomisés menés dans le contexte qui nous intéresse sont monocentriques et de (très) petite taille (24 et 100 patients) et la dernière méta-analyse, regroupant études randomisées et observationnelles, est minée par les biais des études observationnelles, les patients inclus dans les bras ambulatoires de ces études étant évidement moins graves (confusion par indication). Enfin, toutes ces dernières études portent sur la prise en charge ambulatoire par voie veineuse, les études analysant la prise en charge ambulatoire par voie orale étant à ma connaissance inexistantes.
La moitié des décompensations s’installant progressivement sur plusieurs jours ou semaines, on peut envisager d’intervenir précocement pour intercepter le processus avant que le patient ne nécessite une hospitalisation. Le tableau congestif étant moins sévère qu’en cas d’hospitalisation, il faut aussi moins de temps pour faire revenir le patient à un état d’équilibre (qui ne sera pas forcément le même qu’avant l’hospitalisation). Enfin, loin d’être une improvisation, la stratégie ambulatoire peut reposer sur une démarche réfléchie et structurée.
Profil Clinique
Au delà de l’évaluation de la congestion sur laquelle je reviens un peu plus loin, il faut surtout évaluer le risque d’évolution péjorative à court terme. Même si les patients porteurs d’une insuffisance cardiaque en aggravation/en décompensation ont un risque d’évènements plus élevé qu’un patient coronarien, il est possible de trouver de la granularité et d’identifier des patients dont la prise en charge ambulatoire peut se faire en sécurité.
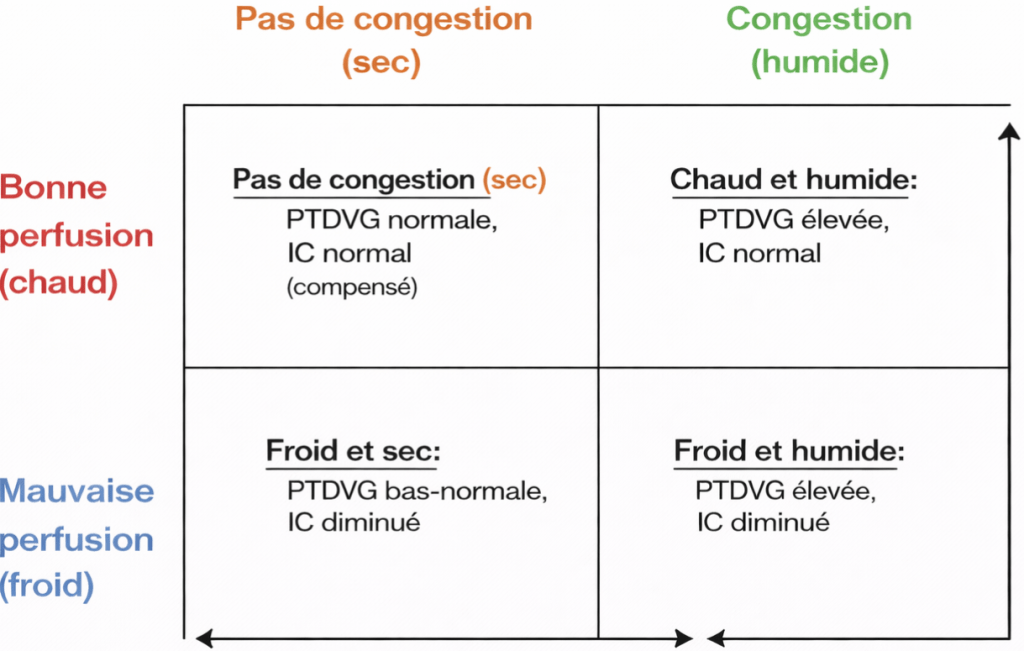
Les profils hémodynamiques identifiés en 1976 par Forester et confirmés par Stevenson dans l’insuffisance cardiaque en 1989 permettent de catégoriser simplement mais efficacement les patients. Ces profils distinguent les patients bien perfusés (« chauds ») de ceux en hypoperfusion (« froids »), et les patients congestifs (« humides ») de ceux sans surcharge (« secs »). Le profil « chaud et humide » – c’est-à-dire un patient congestif mais sans signe d’hypoperfusion représente trois quart des patients présentant une décompensation cardiaque, et ces patients partagent un pronostic à court terme similaire à celui d’un patient stable. Ils représentent donc des candidats idéaux pour une prise en charge en ambulatoire. Au contraire, certains contextes cliniques constituent des contre-indications formelles à une prise en charge ambulatoire, et doivent motiver une orientation hospitalière sans délai.
- Signes d’hypoperfusion (« Profil Froid ») : Tout signe clinique évoquant un bas débit cardiaque (extrémités froides, marbrures, confusion, hypotension symptomatique) impose une prise en charge hospitalière.
- Troubles du rythme ou de la conduction graves : Un bloc auriculo-ventriculaire complet ou une fibrillation atriale rapide et mal tolérée sont des situations à très haut risque qui ne peuvent être gérées en ville.
- Instabilité respiratoire : Une orthopnée sévère, une dyspnée de repos ou un tableau d’œdème aigu pulmonaire nécessitent une prise en charge en milieu hospitalier.
- Facteur déclenchant extrinsèque à haut risque : embolie pulmonaire ou syndrome coronarien nécessitent évidemment une prise en charge hospitalière
L’importance du tableau congestif, et notamment l’importance de la prise de poids, n’est pas en elle-même un critère de gravité. Néanmoins, les congestions importantes peuvent nécessiter de fortes doses de diurétiques et un traitement prolongé, qu’il peut être plus aisé de faire en milieu hospitalier ne serait-ce que pour le recours à la voie veineuse.

Déterminants non cliniques
La décision d’hospitalisation ou de prise en charge ambulatoire ne repose pas uniquement sur des critères cliniques. Des facteurs contextuels, plus subjectifs mais tout aussi importants, doivent être intégrés à l’évaluation pour une décision partagée et une prise en charge sécurisée.
- La préférence du patient : Certains patients préféreront rester à domicile, tandis que d’autres se sentiront plus en sécurité à l’hôpital.
- L’environnement social et familial : Gérer une décompensation chez un patient isolé est bien plus complexe, et risqué, que chez un patient bien entouré, capable de l’accompagner et de l’aider dans la surveillance et l’observance.
- L’environnement médical et paramédical : Bien que ce ne soit pas nécessairement (pour le moment…) un sujet dans notre pays, le coût de l’hospitalisation peut être un frein à la prise en charge hospitalière. Au contraire, l’absence d’infirmière disponible pour prendre le patient à son domicile peut être un obstacle au maintien ambulatoire de certains patients.
- L’expérience du praticien : Le niveau de confort, d’expertise et d’organisation du cardiologue avec la gestion de la décongestion en ambulatoire est un facteur déterminant. Un praticien peu à l’aise avec cette approche ne doit pas se forcer. L’importance du tableau congestif jouera également dans la confiance qu’a le praticien dans une prise en charge ambulatoire. Il m’arrive de faire des décongestions de 10 kg en ambulatoire, mais ce n’est pas chez tous les patients, et ce n’est pas le cas de tous les cardiologues.
Stratégies thérapeutiques ambulatoires
La prise en charge de l’aggravation de l’IC repose sur 3 leviers :
- maîtriser le facteur déclenchant éventuel.
- traiter la congestion
- optimiser le traitement de fond de l’insuffisance cardiaque
Traitement diurétique
A ce jour, aucune étude n’a été menée pour évaluer la prise en charge pharmacologique de l’insuffisance cardiaque décompensée en médecine ambulatoire. En l’absence de données issues d’essais randomisés conduits en ville, la stratégie diurétique ambulatoire repose sur l’extrapolation à partir des études menées en milieu hospitalier, la physiologie rénale et la pharmacologie.

En dehors du traitement diurétique, on insistera classiquement sur la limitation des apports sodés et hydriques. Ce qui, il faut bien l’avouer, ne repose sur aucune donnée (comme il y a plusieurs références concordantes, et pour gagner du temps, je vous mets une diapositive extraite d’un topo que j’ai fait sur le sujet il y a quelques années).
Je ne parlerai pas ici des possibilités de prise en charge par voie intraveineuse (ou sous-cutanée), qui à mon sens sortent du cadre de la question de la prise en charge « au cabinet ». De même, les quelques études qui ont porté sur l’orientation précoce après passage aux urgences vers une prise en charge ambulatoire plutôt qu’une hospitalisation, sortent du champ de ce billet – puisqu’on évalue alors la stratification du risque et l’orientation après prise en charge initiale au SAU, et non pas la prise en charge de la décompensation cardiaque au cabinet du cardiologue. J’en resterai à la prise en charge par voie orale, et je me contenterai d’un tableau synthétique de ce qu’on peut proposer. J’ai longuement abordé le sujet du traitement diurétique de l’insuffisance cardiaque dans plusieurs billets auxquels les lecteurs intéressés pourront se reporter. Le double ou triple blocage néphronique séquentiel est tout à fait réalisable en ambulatoire moyennant l’organisation de la surveillance clinico-biologique – et les gliflozines ne sont toujours pas un traitement de la congestion.
| Classe Thérapeutique | Recommandations Pratiques et Justification Physiologique |
|---|---|
| Diurétiques de l’anse | > 40 mg de furosémide chez les patients naïfs de traitement diurétique. > Doubler la dose orale existante chez les patients déjà sous traitement > Envisager de passer au bumétanide pour sa biodisponibilité supérieure et plus fiable par voie orale, un avantage en cas d’œdème intestinal (1 mg de bumétanide = 40 mg de furosémide) |
| Diurétiques thiazidiques | > Hydrochlorothiazide 25-50 mg > À ajouter en cas de résistance suspectée aux diurétiques de l’anse > Conservent leur efficacité même en cas d’insuffisance rénale sévère. |
| Acétazolamide | > 250 mg 2 fois par jour > Peut être ajouté pour un blocage du néphron proximal > Extrapolation à partir de l’étude ADVOR, qui a démontré l’efficacité de cette molécule par voie IV en milieu hospitalier. |
| Anti-aldostérone | > Spironolactone 25-50 mg > le rôle dans la décongestion aiguë est limité en raison d’un délai d’action long (48-72h) > Ils sont particulièrement pertinents en cas d’hypokaliémie préexistante pour limiter les pertes en potassium. |
Le risque d’hypokaliémie augmente avec la dose et le nombre de diurétiques utilisés. Une supplémentation est souvent nécessaire. On n’oubliera pas que l’hypomagnésémie, favorisée par les diurétiques, entretient l’hypokaliémie. Une supplémentation en magnésium doit être systématiquement envisagée pour corriger la kaliémie plus efficacement.
Traitement de fond
L’aggravation de l’IC doit motiver une réflexion sur le traitement de fond, et tout particulièrement dans l’IC à FEVG altérée pour laquelle les traitements sont clairement identifiés et protocolisés. STRONG-HF a démontré le bénéfice, sur la réduction des évènements cliniques, d’une titration rapide des traitements de fond de l’IC à FEVG altérée dans les suites d’une hospitalisation pour IC aiguë (mais voir l’encart dédié)
STRONG-HF en bref
STRONG-HF (Lancet 2022) a randomisé 1 078 patients hospitalisés pour IC aiguë, comparant une stratégie de titration rapide et intensive des traitements de fond (bêtabloquant, IEC/ARNI, ARM) initiée avant la sortie et poursuivie en ambulatoire, à une stratégie conventionnelle laissée à la discrétion du médecin. Le bras intervention prévoyait quatre visites de suivi rapproché à 1, 2, 3 et 6 semaines après la sortie. Le critère primaire — réhospitalisation pour IC ou décès toutes causes à 180 jours — était significativement réduit dans le bras titration intensive (15,2% vs 23,3%, HR 0,66).
La baisse des évènements a été attribuée à l’intensification rapide et agressive du traitement dans le groupe « intensif ». Cependant les patients à bénéficier de l’intervention étaient surtout les plus jeunes et les moins comorbides – pas tout à fait la population vue en pratique quotidienne. Et si les patients du bras intervention bénéficiaient d’un traitement à doses plus élevées que le bras contrôle, ils avaient un suivi plus rapproché (4 consultations en 6 semaines), qui plus est par des équipes spécialisées dans la prise en charge de l’IC (biais de performance). Il est donc difficile de démêler l’effet propre de la titration de celui du suivi intensif — lequel est une intervention à part entière. Ce n’est pas une raison de ne pas titrer, bien au contraire ; mais c’est aussi une raison de ne pas négliger le suivi.
D’une part, le patient a-t-il toutes les classes thérapeutiques auxquelles il est éligible (bétabloquants ; inhibiteurs de l’enzyme de conversion, antagoniste des récepteurs à l’angiotensine 2 ou sacubitril ; antagoniste des récepteurs minéralocorticoïdes ; gliflozines) ? D’autre part, sont-elles données aux doses maximales tolérées ? Mais aussi, un traitement interventionnel (ablation de fibrillation atriale par exemple) ou électrique (resynchronisation notamment) doit-il être envisagé ? Le patient est-il en insuffisance cardiaque avancée et doit-il être référé à un centre expert pour discuter assistance et/ou greffe ? Ne pas oublier non plus la place de la réadaptation !
Surveillance et Rétrocontrôle
La décision de traiter un patient en ambulatoire engage le praticien à mettre en place un plan de suivi rapproché et structuré. Ce rétrocontrôle est la clé de voûte de la sécurité et de l’efficacité de toute la démarche. C’est peut être ce qui est le plus limitant dans une pratique libérale ambulatoire, car il faut pouvoir réévaluer cliniquement le patient dans les jours qui suivent l’instauration du traitement.
Une réévaluation systématique et précoce du patient est impérative, idéalement dans les 3 à 4 jours suivant l’intensification thérapeutique. Cette consultation de suivi peut être assurée par le cardiologue lui-même ou par d’autres professionnels de santé formés, que ce soient médecins généralistes, infirmières de pratique avancée (IPA) ou infirmières au sein d’un protocole de prise en charge de l’IC (ISPIC), dans le cadre d’un parcours de soins coordonné. Cette réévaluation clinique et paraclinique déclenche une nouvelle décision, créant une boucle de rétrocontrôle.
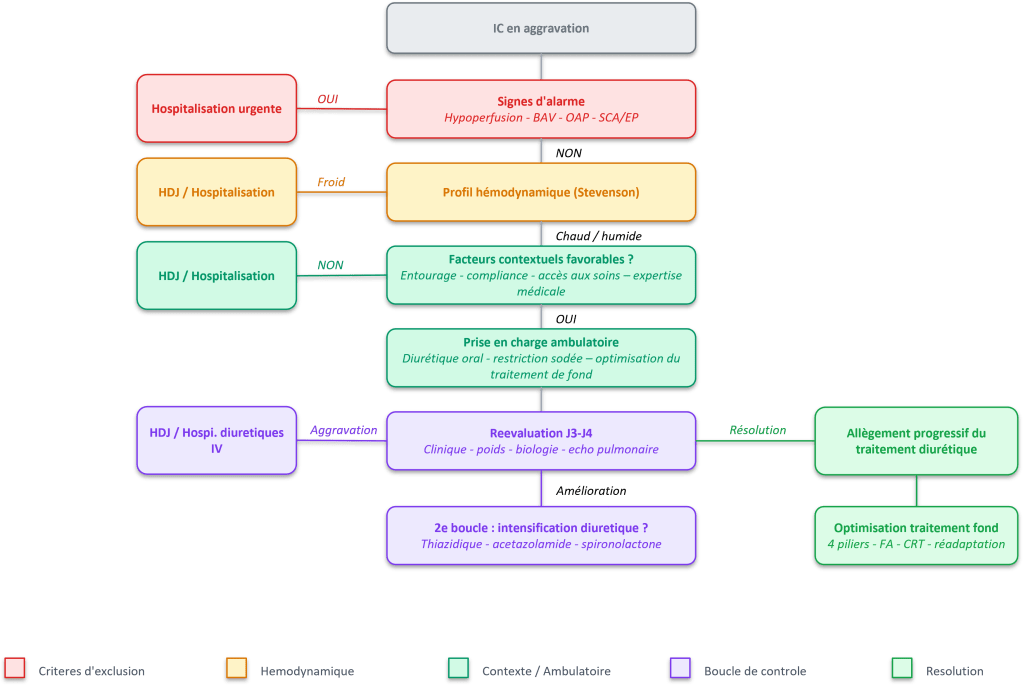
- Si la congestion est résolue : on peut commencer à alléger progressivement le traitement diurétique. La phase de stabilisation peut commencer, avec une attention particulière portée à l’optimisation du traitement de fond.
- Si la congestion est seulement améliorée : soit on poursuit le traitement à l’identique en estimant que la congestion sera résolue dans les jours qui suivent avec le régime diurétique, soit il faut intensifier le traitement diurétique. Dans les deux cas, on entre dans une deuxième « boucle » de la démarche
- Si la congestion est inchangée ou aggravée : Il faut envisager de passer la main et adresser le patient à une structure adaptée (hôpital de jour pour diurétiques IV, hospitalisation conventionnelle).
Plusieurs outils, cliniques et paracliniques, permettent de documenter la réponse au traitement. Néanmoins, ce texte étant déjà long, je ne développerai pas outre mesure le sujet de la surveillance de la décongestion. Il faut cependant souligner qu’il n’y a pas une congestion, mais plusieurs : congestion veineuse (la principale responsable de l’altération de la fonction rénale dans l’insuffisance cardiaque congestive, plutôt que la baisse de la pression de perfusion), congestion tissulaire systémique, congestion tissulaire pulmonaire.
L’Examen Clinique : Même si la sensibilité et la spécificité de l’examen clinique sont modestes, l’évaluation clinique doit être rigoureuse, car c’est parfois le seul outil à notre disposition. La quantification est indispensable pour pouvoir comparer le tableau clinique dans le temps et entre les professionnels prenant en charge la décongestion : hauteur des œdèmes en centimètres, grade de la turgescence jugulaire ou niveau des crépitants
Le Poids : C’est un marqueur simple, fiable, peu coûteux et essentiel. La pesée quotidienne par le patient est un pilier de l’autosurveillance et du suivi, mais également de la télésurveillance. Cet outil est d’ailleurs particulièrement utile pour mettre en place à distance, un suivi quotidien des paramètres clés (poids, pression artérielle, fréquence cardiaque, symptômes).
L’Échographie : La taille de la veine cave inférieure n’a jamais été un indicateur de la volémie et encore moins de congestion ; c’est au mieux un reflet de la pression atriale droite. Il est erroné de penser que l’évolution du diamètre et de la collapsibilité de la veine cave permet de juger de l’efficacité du traitement diurétique. La pertinence du sacro-saint rapport E/e’ mitral pour estimer la pression télédiastolique du ventricule gauche est mauvaise, et c’est tout particulièrement vrai voire même catastrophique en cas de FEVG préservée (où le coefficient de corrélation est de 0,17…). L’échographie pulmonaire est en revanche un excellent outil pour suivre l’évolution de la congestion pulmonaire (lignes B). Mais il y a également l’évaluation des flux veineux notamment rénal, moins évident à réaliser, mais qui apporte des renseignements intéressants.

La Biologie : Un bilan de contrôle (ionogramme, créatininémie) est indispensable pour surveiller la fonction rénale et les électrolytes. J’ajoute volontiers la natriurèse, marqueur de l’efficacité du blocage néphronique, dont la littérature laisse à penser que ce serait un outil intéressant pour guider la décongestion et adapter le traitement diurétique. Cependant, à date, toutes les études ont été faites en milieu hospitalier sur la base de natriurèse prélevées sur échantillon deux heures après l’initiation/l’adaptation du traitement diurétique, et aucune étude ne nous renseigne sur l’apport de ce dosage en pratique ambulatoire. On pourrait néanmoins imaginer une mesure de la natriurèse à la deuxième heure sur échantillon urinaire au cabinet grâce à un analyseur spécifique ; EASY-HF a montré la faisabilité d’un tel protocole. En revanche, le suivi des peptides natriurétiques n’apporte aucun bénéfice pour guider l’ajustement du traitement diurétique durant la phase de décongestion. C’est probablement le fait que de nombreux facteurs viennent modifier la concentration plasmatique de BNP/NT-proBNP à court terme, notamment le débit de filtration glomérulaire ou la fibrillation atriale.
Conclusion : Vers un Parcours de Soins Intégré et Standardisé
L’enjeu n’est donc pas de choisir entre la ville et l’hôpital, mais de construire un système de soins intégré où chaque patient est orienté vers la structure la plus pertinente en fonction d’un processus décisionnel partagé et rigoureux. La prise en charge de la décompensation cardiaque en ambulatoire est non seulement possible mais est déjà une réalité pour une part significative des patients. Le choix du lieu de soin doit être avant tout guidé par une stratification rigoureuse du risque. La détection de signes d’hypoperfusion ou d’instabilité respiratoire reste le critère d’exclusion principal et non négociable de la prise en charge ambulatoire. La qualité et la sécurité des soins en ville reposent sur la standardisation du processus : une évaluation clinique et paraclinique structurée, un plan d’action thérapeutique réfléchi et, surtout, une réévaluation précoce sont obligatoires.
Loin d’être une option par défaut, la prise en charge ambulatoire de la décompensation cardiaque est une stratégie pertinente et sûre si elle est maîtrisée et correctement encadrée. Congestion n’est pas synonyme d’hospitalisation !

Super !! Merci beaucoup.
Tu pourrais éventuellement nous en dire plus sur « l’allègement progressif du traitement diurétique », en ce qui concerne les diurétiques de l’anse ? En effet, on voit souvent des diminutions de posologie qui m’ont toujours paru curieuses étant donné la pharmacodynamie en sigmoïde suivant une loi du « tout ou rien » approximative (hors syndrome cardiorénal même a minima).
Faut-il considérer qu’à un état de congestion donné correspond une dose bien précise de diurétique de l’anse efficace, et qu’une fois la décongestion initiée il faut conserver la même dose jusqu’à décongestion satisfaisante, ou tu penses que la réalité est moins tranchée et justifierait une diminution progressive des doses ?
J’aimeJ’aime
Comme on n’a pas vraiment d’étude bien faite sur le traitement diurétique pour la décongestion, autant dire qu’on n’a aucune donnée sur la décroissance thérapeutique !
Mon expérience est de faire du doigt mouillé, en fonction de l’importance de la congestion initiale, du niveau de décongestion au moment de la consultation, du régime diurétique et blocage néphronique en cours, de la fonction rénale, etc… Je baisse souvent par palier de moitié de dose, en cherchant la dose minimale efficace (voir l’arrêt du diurétique de l’anse). Si la baisse s’accompagne d’une reprise pondérale et congestive même discrète, je remonte un peu la dose. Mais je n’ai jamais réfléchi à un protocole bien cadré de diminution de dose
Dans l’IC à FEVG préservée, dans laquelle les besoins en diurétiques sont moins importants, j’aime beaucoup passer à SPIRONALACTONE/ALTIZIDE afin de garder un traitement diurétique de fond s’il est nécessaire sans multiplier le nombre de comprime
J’aimeJ’aime
Merci pour ce double billet qui est très clair et qui trace bien la route. Mais comme tu le dis, ce type de prise en charge en ambulatoire parait très très difficile à mettre en place dans le contexte actuel des soins en ville. Les rendez-vous avec les Cardiologues varient de 1 à 3-4-5 mois, ce qui en dit long sur leur emploi du temps et leur disponibilité. Et pour les Médecins Généralistes ils ont les mêmes obstacles de temps et de disponibilité et un manque cruel de formation pour ce type de prise en charge (complexe et compliquée) et la manipulation des différentes drogues à utiliser. Reste que tes arguments sont convaincants
J’aimeJ’aime
J’arrive à faire ce genre de prise en charge parce que
– je travaille avec un IPA qui prend en charge le suivi de nombreux patients, notamment les patients avec insuffisance cardiaque stabilisée, l’équilibration d’un traitement antihypertenseur, le contrôle d’une décongestion, etc…
– je limite au maximum les consultations de suivi inutiles : pas de consultation annuelle systématique pour une hypertension artérielle ou un diabète équilibré asymptomatique, pas d’échographie ou de tests d’effort systématiques « pour voir », etc…
– j’ai 3 créneaux laissés libres dans la semaine pour pouvoir répondre à ce besoin.
J’aimeJ’aime