J’ai eu le plaisir de participer lors des Journées Francophones de l’Insuffisance cardiaque, des Cardiomyopathies, de l’Assistance et de la Transplantation, en septembre 2025 à Poitiers, à une controverse autour de la possibilité de traiter les décompensations cardiaques en médecine de ville. Après que j’ai – évidement – argumenté en faveur de cette prise en charge, Diane Bodez a réfuté cette possibilité. Naturellement, mauvaise foi et exagération dans chaque camp sont les clefs d’une controverse réussie. Jean-Michel Tartière a finalement « réconcilié » tout le monde dans une troisième présentation. Merci à eux deux, ainsi qu’à Anne Flore Plane et Barnabas Gellen qui ont modéré cette session en ne manquant pas de relancer les débats quand ils s’essoufflaient un peu. Plutôt qu’un compte rendu individuel de chacune des interventions, je vous propose ici une synthèse de ces échanges fructueux.
(Venez au JFIC-CAT, c’est un congrès extra, plein de bonne humeur ; on sera à Toulouse en septembre 2026)
Introduction
L’hospitalisation est un évènement extrêmement fréquent dans l’évolution de l’insuffisance cardiaque (IC), à tel point que la majorité, si ce n’est tous les patients ayant une insuffisance cardiaque, sera hospitalisée au moins une fois au cours de l’évolution de la maladie. Dans une étude publiée par F. Beauvais pour le GICC en 2021, des symptômes d’IC étaient déjà présents depuis plus de 15 jours chez près de la moitié des patients hospitalisés pour IC, et chez un tiers des patients depuis plus de 2 mois. Pour moitié d’entre eux, les patients passant par les urgences pour une dyspnée cardiogénique ont une insuffisance cardiaque déjà connue. On voit donc que nombre de patients hospitalisés pour une IC décompensée pourraient être identifiés plus tôt et, partant, être éventuellement pris en charge en ambulatoire (c’est d’ailleurs sur la base de ces réflexions que s’est développée la télésurveillance dans l’IC). La pratique habituelle de recourir à l’hospitalisation en cas de décompensation cardiaque est-elle obligatoire ? Ne peut-on envisager des prises en charge alternatives, ambulatoires ? Peut-on imaginer un cadre décisionnel structuré pour proposer un parcours de soin ambulatoire sécurisé ?
Définitions
On a longtemps considéré l’IC comme présentant deux formes cliniques, chronique ou aiguë, la première relevant du suivi ambulatoire et la seconde de la prise en charge hospitalière. Comme si la décompensation cardiaque ne pouvait exister que comme un tableau clinique bruyant et d’installation rapide. Or le terme d’IC aiguë est impropre dans de nombreuses circonstances, car le passage d’un état stabilisé (plutôt que stable) à un état décompensé est le plus souvent progressif sur des jours ou des semaines, avant que les patients ne reçoivent finalement un traitement en urgence (ou aux urgences…). Les grands essais cliniques considéraient habituellement la seule hospitalisation pour IC décompensée comme critère de jugement ; la nécessité de majorer le traitement diurétique en raison de l’installation d’un tableau congestif était d’autant plus ignorée si la prise en charge avait était efficace et avait prévenu l’hospitalisation.
Bien que le concept soit plus ancien (il est notamment mentionné dans les recommandations européennes de 2008) et connu de longue date en pratique quotidienne, notamment en médecine ambulatoire, on doit probablement à Greene, en 2018, la conceptualisation et diffusion dans la littérature de l’idée de Worsening Heart Failure. Par la suite, nombre d’articles ont étudié cette population jusque là globalement ignorée dans les essais.
Cadre Nosologique
L’établissement d’une définition claire et partagée du concept d’aggravation de l’insuffisance cardiaque est essentiel pour cadrer la discussion clinique, favoriser la recherche et évaluer les pratiques. Les définitions proposées par les sociétés savantes européennes et américaines sont aujourd’hui globalement homogènes. On définit donc l’aggravation de l’insuffisance cardiaque comme :
L’aggravation, après une période de stabilité, chez un patient avec une insuffisance cardiaque chronique, des signes et symptômes d’insuffisance cardiaque, nécessitant l’augmentation des traitements
Cette définition demande quelques précision.
Présence de signes et symptômes : apparition ou aggravation de signes et de symptômes caractéristiques de l’insuffisance cardiaque (dyspnée, œdèmes, orthopnée). Les signes et symptômes seuls manquant de sensibilité et de spécificité, la suspicion diagnostique sera utilement étayée par le dosage des peptides natriurétiques ou l’évaluation hémodynamique échographique en cas de doute diagnostique (ne me faites pas dire ce que je n’ai pas écrit : les peptides natriurétiques ou même l’échographie sont inutiles pour poser le diagnostic devant un patient ayant une insuffisance cardiaque connue, présentant une prise de poids de 5 kg avec un œdème remontant aux genoux et un reflux hépatojugulaire à 10 cm persistant en inspiration). On peut après tout rassembler sous le vocable signes des élements cliniques et paraclinique comme des signes échographiques de congestion (ligne B pulmonaire, flux veineux rénal biphasique, etc…).
Intensification thérapeutique : Le tableau clinique doit nécessiter une intensification du traitement. Pour certains, seule l’administration intraveineuse entre dans la définition. Cependant, de plus en plus d’essais cliniques ou d’analyses ancillaires intègrent un critère de jugement en lien avec les épisodes congestifs pris en charge en ambulatoire, donc par voie orale (voir plus bas). De manière intéressante, la définition repose donc avant tout sur le traitement (ou plutôt le changement de traitement), plus que sur la physiopathologie sous-jacente. De même, la définition est indépendante de la voie (orale ou intraveineuse) ou du lieu de l’administration des traitements (ambulatoire, service d’urgence, hôpital de jour, etc.) – qui vont dépendre de paramètres non médicaux – comme la disponibilité des ressources ou des incitations financières – ou médicaux comme l’expérience du praticien. La question qui n’est cependant pas résolue est celle de l’importance de l’augmentation du traitement qui défini l’insuffisance cardiaque en aggravation : faut-il considérer une augmentation relative ou absolue de la dose de diurétiques ? un ajout de 20 mg, 40 mg de furosémide ? un doublement de la dose ? l’ajout d’un deuxième diurétique ?
Ambiguïtés Pratiques
Bien que le cadre nosologique semble bien délimité, la pratique quotidienne et l’hétérogénéité des présentations cliniques imposent de nuancer la définition, ou au moins de la confronter à la complexité du réel. Cette hétérogénéité des profils de patients et des scénarios cliniques rend la stratification du risque d’autant plus cruciale pour orienter la décision thérapeutique.
Temporalité
Un tableau aigu s’installant en 24 heures, menant le plus souvent à un appel au SAMU, n’a rien de commun avec une congestion progressive s’étalant sur plusieurs jours, voire plusieurs semaines. De plus, la définition insiste sur l’existence d’une période de stabilité avant l’apparition des symptômes, mais n’en précise pas la durée. Dans quelle mesure un patient présentant une aggravation clinique dans les jours/semaines suivant une hospitalisation pour IC présente-t-il une aggravation de l’IC plutôt qu’une rechute de l’IC ayant conduit à la première hospitalisation ? Si cette apparente subtilité ne change pas nécessairement la prise en charge au regard des connaissances actuelles, la question est tout autant sémantique que physiopathologique voire pronostique.
Facteur déclenchant
La prise en charge est différente entre un patient confronté à un facteur déclenchant extrinsèque réversible et identifiable (infection, écart de régime, arrêt transitoire du traitement, …), et un patient traité de manière optimale et observant, dont l’aggravation est la traduction d’une progression intrinsèque de la maladie sans facteur déclenchant identifié. Dans le premier cas, la maîtrise du facteur déclenchant est indispensable à la prise en charge. Ce facteur déclenchant peut d’ailleurs être une mauvaise adhérence thérapeutique. Le second cas impose d’interroger la prise en charge de fond et d’envisager une escalade/optimisation thérapeutique. Notamment dans la situation malheureusement fréquente, où le patient ne reçoit pas tous les traitements (pharmacologiques ou non) et/ou les doses auxquelles il est normalement éligible (sous-traitement et sous-dosage).
Si la définition suppose donc implicitement que l’état clinique s’est aggravé malgré un traitement optimal bien conduit et bien suivi, doit-on différencier insuffisance cardiaque en décompensation quand il existe un facteur externe et/ou un traitement de fond insuffisant et insuffisance cardiaque en aggravation quand la tableau congestif s’installe malgré un traitement optimisé et en l’absence de facteur déclenchant externe ?
Note sémantique
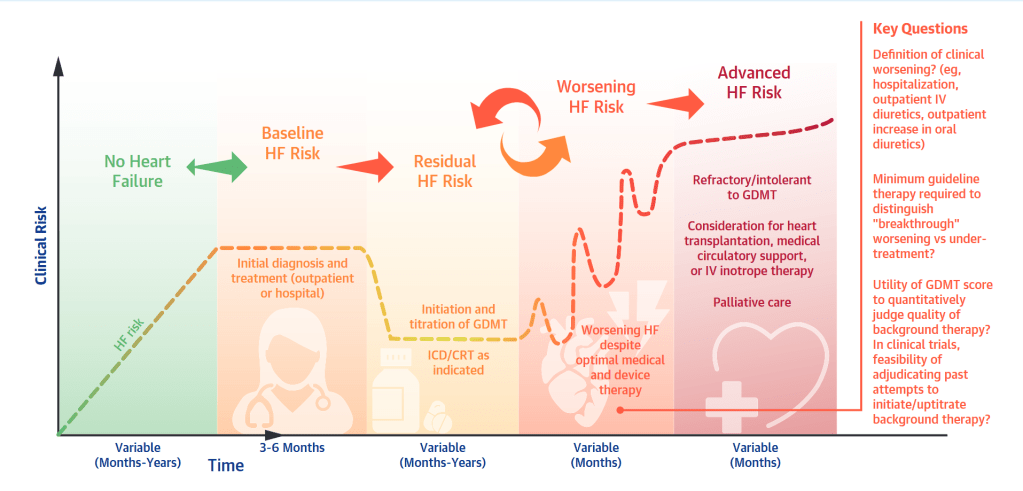
Le terme worsening heart failure se traduit naturellement par « insuffisance cardiaque en aggravation » ou « aggravation de l’insuffisance cardiaque ». Si la définition suppose implicitement que l’état clinique s’est aggravé malgré un traitement optimal bien conduit et bien suivi, il faudrait différencier insuffisance cardiaque en décompensation (facteur décompensant extrinsèque identifiable) et insuffisance cardiaque en aggravation (progression intrinsèque de la maladie). La distinction est cependant artificielle en pratique : il est le plus souvent impossible de faire la part des choses au moment du diagnostic du tableau congestif, entre un facteur décompensant extrinsèque et une progression intrinsèque. On demanderait à une entité clinique d’orienter une prise en charge alors même qu’elle est définie non par un substrat physiopathologique mais par cette même prise en charge. Soulignons également que si dans la définition « intensification des traitements » est habituellement compris comme « les traitements diurétiques » (et c’est d’ailleurs le cas dans l’article de Greene de 2023), on peut tout autant l’entendre comme « intensification des traitements de fond de l’insuffisance cardiaque ». L’aggravation de l’insuffisance cardiaque serait ainsi tout autant un évènement aigu ou subaigu (intensification diurétique, temporalité courte), ce qui correspond à l’usage dominant dans la littérature et notamment dans les essais cliniques, et auquel on se réfère habituellement sous le terme de « décompensation cardiaque » ; qu’une phase plus longue (intensification du traitement de fond, progression de la maladie) qui ferait la transition entre une insuffisance cardiaque stabilisée et l’insuffisance cardiaque avancée. Cette phase correspond à ce que Greene illustre dans la Figure 3 de son article de 2023 (voir ci-dessous) et elle appelle une réflexion sur les optimisations thérapeutiques de fond : pharmacologiques, mais aussi interventionnelles et de réadaptation.
Contexte clinique
Il faut distinguer l’aggravation d’une maladie chronique connue (qui est le sujet de ce texte) d’une décompensation de novo amenant à la découverte d’une IC. On sort alors du cadre de l’aggravation pour entrer dans celui de la prise en charge initiale thérapeutique et diagnostique de l’IC. Là encore la prise en charge du tableau congestif en lui-même ne sera pas différente de celle d’un patient déjà connu pour son insuffisance cardiaque (encore que la question d’une résistance aux diurétiques ne se posera pas), mais il s’agira d’assurer en parallèle la prise en charge initiale de la maladie chronique.
Épidémiologie
Première certitude, l’aggravation de l’insuffisance cardiaque est un évènement fréquent. Cela concerne par exemple 9 évènements sur 100 patients-années dans un registre danois. Dans une étude américaine, un quart des tableaux d’IC en aggravation était pris en charge en ambulatoire. La fréquence de prise en charge ambulatoire augmente de manière continue depuis 2012 (3,3 épisodes d’aggravation d’IC traités en ambulatoire pour 100 patients-années en 2012 et 9,7 en 2019), alors que les prises en charge hospitalières (aux urgences ou en hospitalisation) sont stables. Dans DAPA-HF, la première manifestation de l’IC après la randomisation est une décompensation cardiaque prise en charge en hospitalisation pour 10,3% des patients, et une décompensation cardiaque prise en charge en ambulatoire pour 8,6% des patients. Dans DELIVER, la proportion est inversée (9 et 13% respectivement). Dans VICTOR, la première manifestation de la dégradation de l’IC est majoritairement (59%) prise en charge en ambulatoire.
Au moment de la décompensation, les patients hospitalisés sont globalement plus graves que les patients ayant une congestion cardiogénique prise en charge en ambulatoire. Naturellement, que ce soit dans DAPA-HF, DELIVER ou BIOSTAT, le pronostic des patients hospitalisés est bien plus sombre que celui des patients pris en charge en ambulatoire ; non pas, évidemment, que l’hospitalisation soit délétère, mais bien parce que les plus graves sont hospitalisés – il y a d’ailleurs une corrélation entre l’importance de l’augmentation de la dose de furosémide et aggravation du pronostic (et là encore par biais de confusion par indication : les patients les plus graves ont besoin d’une dose plus importante de diurétique et sont ceux qui meurent le plus, ce qui ne veut pas dire que les diurétiques soient des médicaments particulièrement dangereux – comme certains ont pu le suggérer à une époque)
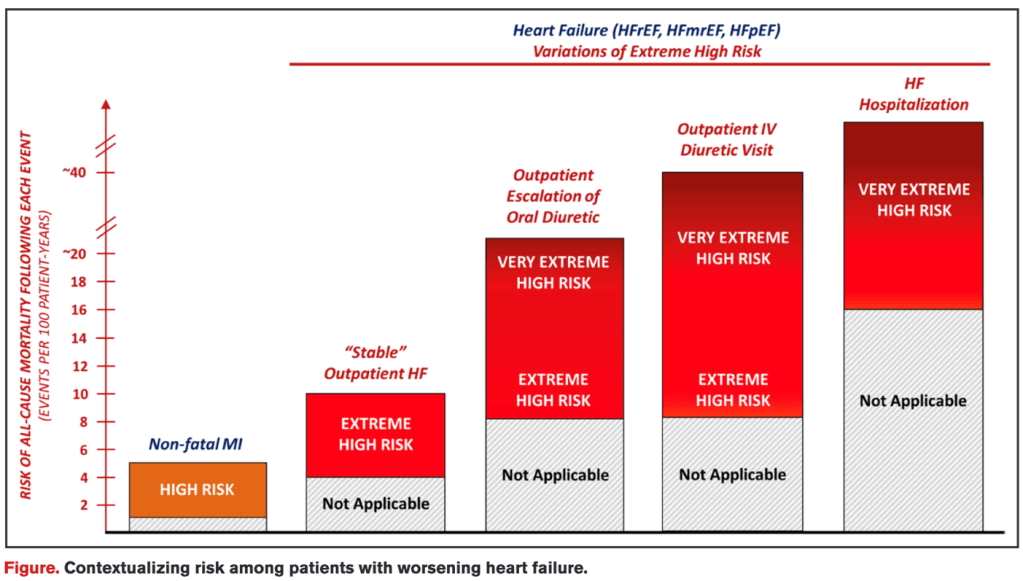
Pour autant, l’aggravation de l’insuffisance cardiaque, même prise en charge en ambulatoire, n’est absolument pas un évènement anodin. Certains patients parmi les plus sévères pris en charge en ambulatoire ont un risque de mortalité similaire aux patients hospitalisés. Dans le registre danois mentionné plus haut, la nécessité d’augmenter la dose de diurétique pris par voie orale est associée à une augmentation de la mortalité dans l’année de 75% (ce ne sont toujours pas les diurétiques qui sont dangereux…). Dans DAPA-HF ou DELIVER, le risque de mortalité totale est multiplié par 2 à 3 en cas d’aggravation de l’IC prise en charge en ambulatoire (et par 8 en cas d’hospitalisation). Le pronostic de ces patients est de loin plus mauvais que les patients ayant une IC stabilisée, et sans commune mesure avec un patient ayant fait un infarctus du myocarde. La nécessité de majorer le traitement diurétique n’est donc pas un évènement anodin dans le parcours de soin d’un patient porteur d’une IC.
Conclusion
L’aggravation de l’insuffisance cardiaque est un événement fréquent, grave sur le plan pronostique, et déjà pris en charge en ambulatoire pour une part significative des patients. La question n’est donc pas tant de savoir si cette prise en charge est légitime, mais de se donner les moyens de la faire correctement et en sécurité. Les ambiguïtés sémantiques reflètent la complexité d’une entité clinique en cours de définition, et rappellent que la rigueur terminologique est une condition nécessaire pour comparer les pratiques, interpréter les essais, et progresser collectivement. Ignorer ces épisodes ambulatoires sous-estime le fardeau de la pathologie et fait rater des occasions d’optimiser la prise en charge de fond de l’IC.
Dans un second billet, nous verrons comment structurer la démarche de prise en charge : identifier le patient adéquat pour une prise en charge ambulatoire, adapter le traitement diurétique par voie orale, et surveiller efficacement pour ne pas rater une dégradation.

Merci pour votre travail d’explication et d’analyse. Sans avoir la prétention de tout saisir, ça permet de réfléchir à ses pratiques. Continuez car vous transmettez au delà de votre propre spécialité ! Bien confraternellement.
J’aimeAimé par 1 personne