La Société Française de Diabétologie a publié en novembre sa dernière mise au point sur la prise en charge du diabète de type 2 (DT2). La liste des liens d’intérêt des auteurs est longue comme le bras, mais il n’est fait nulle part mention de niveau de preuve pour étayer chacun des avis. Pour autant, on a quelques évolutions timides mais intéressantes dans les concepts qui guident le traitement pharmacologique. J’en ai fait une publication sur LinkedIn, en mentionnant au passage l’étude UKPDS.
UKPDS : nombreux sont les médecins a avoir déjà entendu parler de cette étude. UKPDS (pour United Kingdom Prospective Diabetes Study) est un vaste programme de recherche clinique britannique visant à définir la stratégie thérapeutique optimale dans le DT2. Il s’agit d’une étude randomisée, ayant inclus plus de 5.000 patients, suivis pendant 20 ans (1977 à 1997). Tous les protocoles de traitements du DT2, et notamment la place centrale de la metformine, reposent sur les résultats d’UKPDS. Mais pour autant que la metformine soit largement recommandée et utilisée en première ligne de traitement, et UKPDS allègrement citée comme démonstration scientifique de son efficacité thérapeutique, qui a vraiment lu UKPDS ? A en croire la célébrité de cette étude, et la référence absolue qu’est la metformine dans le DT2, il est évident qu’UKPDS est un programme d’étude clinique bien conduit et méthodologiquement robuste, dont on peut tirer des conclusions sans hésitation. Si seulement…
La place de la metformine a été évaluée dans UKPDS-34, publiée en 1998 dans le Lancet. Oui, il y a bien eu 33 autres papiers basés sur UKPDS avant celui sur la metformine ; et il y en a eu beaucoup d’autres après… vous pouvez trouver la liste ici. UKPDS-33, par exemple, comparait traitement par sulfamide ou insuline vs régime seul. En quoi consiste UKPDS-34 : Entre 1977 et 1991, des patients atteints de DT2 nouvellement diagnostiqué, âgés de 25 à 65 ans, présentant deux glycémies à jeun consécutives supérieure à 6,0 mmol/L, ont été invités à suivre un régime riche en glucides et en fibres, pauvre en graisses saturées, avec une restriction énergétique pour les patients en surpoids. Après 3 mois de régime, 4 209 patients éligibles présentant une glycémie à jeun supérieure à 6,0 mmol/L ont été randomisés entre « traitement conventionnel » par régime seul, ou « traitement intensif » par sulfamide hypoglycémiant ou insuline (c’est UKPDS-33), la metformine constituant une option thérapeutique pour les patients en surpoids (c’est UKPDS-34). Mais seulement 15 centre sur les 26 d’UKPDS-33 participent à UKPDS-34. On a donc deux études imbriquées l’une dans l’autre, dont l’une ne concerne qu’une partie des centres ; mais c’est encore trop simple… Car il y a plusieurs randomisations dans UKPDS-34.
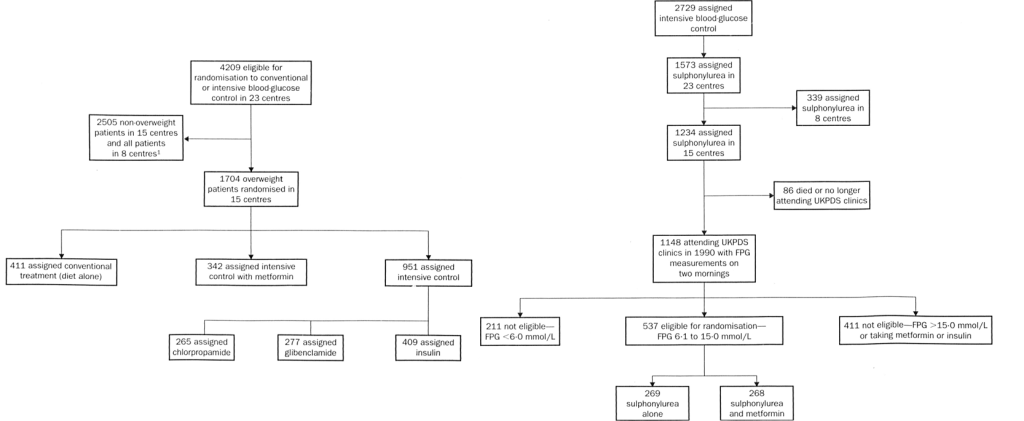
- Une première randomisation chez des patients obèses permettant d’avoir 342 patients sous metformine, 411 sous régime seul et 951 sous insuline ou sulfamide.
- Les 411 patients sous régime pouvaient être secondairement randomisés en cas de contrôle glycémique imparfait et donc recevoir ou de la metformine, ou de l’insuline, ou un sulfamide. Et si les patients sous sulfamide restaient hyperglycémiques (après la première ou la deuxième randomisation), la metformine pouvait être ajoutée (sans randomisation…). Si les patients initialement sous metformine n’était pas contrôlés au plan glycémiue, du glibenclamide était ajouté.
- Une troisième randomisation concernent les patients sous sulfamides dans UKPDS-33 et inclus dans l’un des 15 centres retenus dans UKPDS34, et dont le contrôle glycémique n’est pas optimal (vous suivez ?). Ces patients étaient alors randomisés entre ajout de metformine ou poursuite du sulfamide, ce dernier groupe pouvant quand même se voir adjoindre de la metformine en cas d’hyperglycémie persistante.
Vous êtes perdus ? c’est normal. On a deux flowchart dans UKPDS-34 puisque ce sont deux études différentes. Après l’analyse sur les 1704 patients obèses, les populations des deux études sont fusionnées pour une analyse commune ; a aucun moment est-on certain que les patients n’ont pas été comptés deux fois, compte tenu des changement de bras et de traitements, des centres inclus ou non dans l’analyses, etc.. Le nombre de patients par groupe ne correspond pas entre UKPDS-33 et 34, mais rien ne peut être vérifié, puisqu’on a 26 centres dans l’une des études, et seulement 15 centres dans l’autre. Enfin, l’attrition est vertigineuse : Sur les 1704 patients initiaux d’UKPDS-34, on n’en a plus que 857 à 10 ans, et 92 (!) à 15 ans.

Les critères de jugement sont tellement nombreux que je vous mets une capture d’écran. Notez que l’étude n’est pas menée en aveugle et que de nombreux critères sont sensibles à des biais en l’absence d’aveugle – ne serait-ce que les décès de causes spécifiques. Me direz-vous, quand on est perdu dans une étude, le mieux est d’en revenir à la base : le protocole. Mais il n’y a pas de protocole initial ! Le protocole a été publié en 1991 (pour une étude débutée en 1977), avec notamment la présentation du nombre d’évènements déjà survenus pour chaque critères de jugement (table 4) ! On croit en outre comprendre que certains critères de jugement ont été ajoutés à posteriori, par exemple la photocoagulation, dont les critères de recours ne sont pas défini précisément ; critère de jugement au demeurant sensible à l’absence d’aveugle – si je puis me permettre… . je passe sur le fait que les analyses statistiques étaient faites de manières itératives tous les 6 mois, sans ajustement ni précautions méthodologiques (après tout, qui se soucie de l’inflation du risque alpha ?).
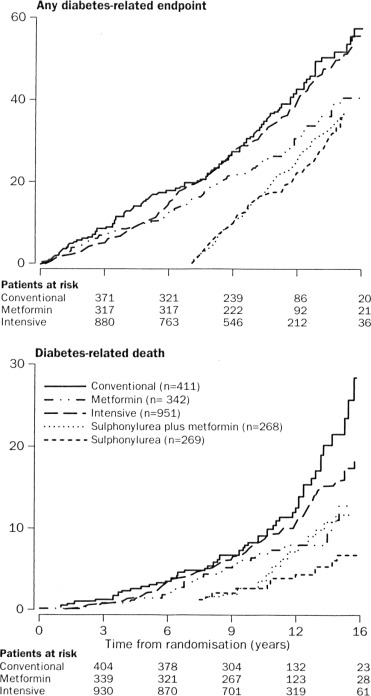
Mais alors, la metformine, ça fonctionne ? Quand on analyse un petit sous groupe de patients (342 patients obèses sous metformine sur 4209 patients dans l’ensemble d’UKPDS), et qu’on multiplie les analyses sans ajustement statistique, on arrive à trouver que la metformine permet une diminution des multiples critères fourre-tout de jugement, chez les patients obèses, en comparaison du bras « diététique seul » (qui ne comprend lui que 411 patients) : baisse de 32 % (IC95% 13 – 47, p = 0,002) des évènements liés au diabète, de 42 % de la mortalité liée au diabète (IC95% 9 – 63, p = 0,017), et de 36 % de la mortalité toutes causes (IC95% 9 – 55, p = 0,011). Notez au passage les valeurs de p, alors que les auteurs précisent dans UKPDS-33 que la significativité statistique a été modifiée en cours d’étude, passant de p < 0,01 à p < 0,05 ; les bénéfices sur les mortalités liées au diabète et toutes causes n’auraient donc pas été significatifs si on s’en tenait au protocole « initial » (qu’on n’a pas, je vous le rappelle). Pour une étude en ouvert aussi longue, on devrait en outre pouvoir analyser la prise en charge des autres facteurs de risque, notamment maladie rénale et hypertension artérielle – les statines n’existaient pas – et de s’assurer que les traitements et la maîtrise des facteurs de risque soient comparables dans les groupe (sans quoi on ne peut exclure que le bénéfice ne soit pas en fait lié à cette meilleure prise en charge) ; nous n’avons malheureusement pas cette information, et l’absence d’aveugle est en soit un risque de déséquilibre dans la prise en charge des autres facteurs de risque.
Dans un deuxième temps, les patients issus des différentes randomisations sont regroupés pour former une seule étude (avec de nouvelles analyses…) et des groupes traitement diététique, metformine, insuline, sulfamide, ou traitement combiné, et « démontrer » ainsi l’avantage du traitement intensif par rapport au traitement diététique. Il y a cependant un autre résultat dont on parle assez peu. L’ajout de metformine à un sulfamide est associé à une augmentation du risque de mortalité lié au diabète de 96 % (p = 0,039) et du risque de décès toutes causes confondues de 60 % (p = 0,041). Bizarrement, ce résultat très défavorable est systématiquement passé sous silence et/ou attribué au hasard, alors que le résultat principal est évidement une preuve scientifique solide basée sur une méthodologie robuste.
On voit donc qu’UKPDS-34 cumule de lourds problèmes méthodologiques : protocole initial non publié, analyses intermédiaires itératives, critères de jugement multiples et composites, multiplication des bras et protocoles de traitement, modification des critères de jugement et changement des seuils de significativité, changement de traitement et de bras en cours d’étude, absence de placebo et d’aveugle, analyses statistiques multiples sans ajustement, sous groupe de faible effectif, attrition sévère, etc… Aucune molécule ne serait utilisée si un tel essai était publié de nos jours. Dans un article publié en 2016 dans le British Medical Journal, Remy Boussageon lève encore quelques autres points méthodologiques et souligne surtout que les résultats positifs d’UKPS-34 n’ont jamais été répliqués, alors que le surrisque de l’association metformine + sulfamide a, lui, bien été documenté. Un méta-analyse parue l’année d’après ne parvient pas non plus à démontrer une baisse des évènements sous metformine ; mais moins de 3.000 patients ont été inclus dans 13 études, illustrant la multiplication d’études de petite taille avec un un faible nombre d’évènements.
L’absence de preuve n’est pas la preuve de l’absence, mais il est fondamental de rappeler que cette molécule, même si elle est très bon marché, n’a jamais été correctement évaluée. Et ce n’est pas avec des études observationnelles qu’on démontre l’efficacité d’un traitement. Son statut de « première ligne » thérapeutique repose largement sur UKPDS dont on voit les profonds problèmes méthodologiques et les conclusions contestables, et sa prescription « réflexe » est plus dogmatique que basée sur des données solides. Son profil de tolérance (troubles digestifs, acidose lactique rare) n’est pas anodin, et les données de bénéfice cardiovasculaires bien moins robustes (pour ne pas dire inexistantes) comparées aux nouvelles classes. Il est tout aussi fondamental de souligner qu’il y a un risque dans l’association metformine + sulfamide ; ce n’est pas la première fois que je l’écris, mais je persiste à penser que cette classe devrait être déremboursée (note aux patients qui liraient ces lignes : n’arrêtez pas vos traitements sans l’avis de vos médecins).
A l’heure où on a enfin dépassé le concept des traitement hypoglycémiants (qui font baisser l’HbA1c sans diminuer les évènements) pour voir arriver des traitements antidiabétiques (qui améliorent le pronostic clinique sans forcément faire baisser l’HbA1c), il serait bon que les recommandations évoluent et arrêtent de mettre en première ligne un traitement sans efficacité démontrée. Un doux rêve de cardiologue un peu trop à cheval sur la méthodologie ? Jetez un œil aux recommandations 2026 de l’American Diabetes Association…

C’est tout de même franchement angoissant.
Outre les biais temporels qui font que certaines thérapeutiques mériteraient de nouveau d’être challengé, de se rendre compte de la pauvreté méthodologique dont nos pratiques peuvent découler…
Et surtout, quoi en faire derrière ça ? Déprescrire la METFORMINE chez tout le monde ?
J’aimeJ’aime
Déprescrire la metformine, non. Mais déjà arrêter d’en faire l’alpha et l’oméga de la base du traitement ; et arrêter d’enseigner UKPDS sans vision critique.
Quand à la pauvreté méthodologique de certaines études et des fondements instables de bien des pratiques, c’est un vaste sujet. Que certains n’aiment pas trop voir aborder
J’aimeJ’aime
[…] avec un bénéfice clinique démontré, iSGLT2 et bloqueurs du SRA, pour la métformine, je vous laisse lire ça. Pour les diurétiques, ça dépend de leur usage. Pour les AINS, vous pouvez les arrêter […]
J’aimeJ’aime